As funções orgânicas são os grupos de compostos químicos com propriedades físico-químicas semelhantes por conta de suas estruturas, que contêm um grupo funcional em comum. Esses grupos são a sequência de átomos que compõem parte da molécula, específicos de cada função orgânica. O grupo funcional garante ainda uma nomenclatura específica para cada função. Veja como identificá-lo a seguir!
Publicidade
Como identificar uma função orgânica?
Para tal, é preciso estudar a estrutura de uma molécula na busca de um grupo funcional conhecido. A partir disso, analisando os átomos presentes e o tipo de ligação existente entre eles, é possível determinar o tipo de função orgânica da molécula em questão, além da nomenclatura correta dela.
Relacionadas
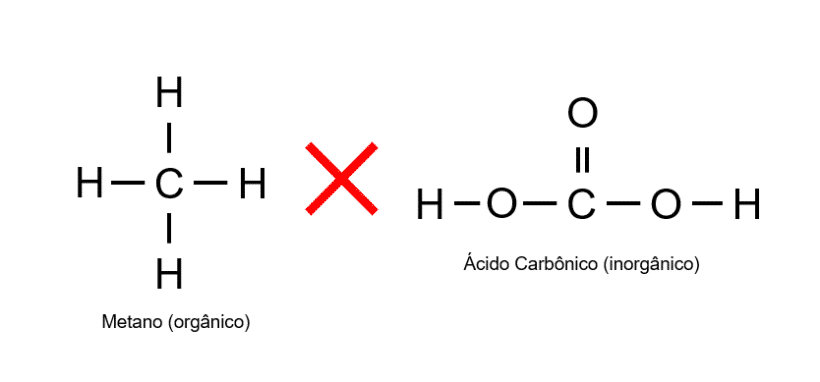
De modo geral, os compostos orgânicos se diferenciam dos compostos inorgânicos por apresentarem átomos de carbono diretamente ligados aos átomos de hidrogênio ou distribuídos em uma longa cadeia carbônica. Um exemplo dessa diferença é o metano (CH4) e o ácido carbônico (H2CO3):
Principais funções orgânicas
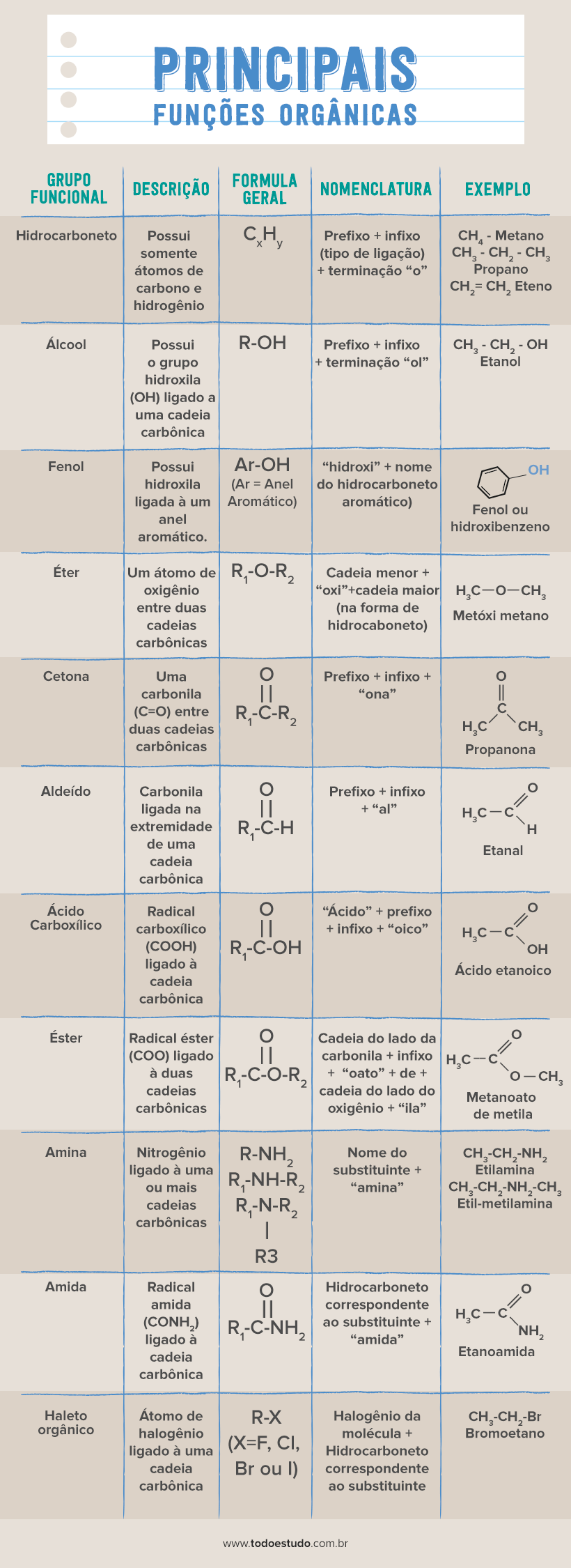
Existem mais de 50 funções orgânicas diferentes, mas apenas algumas delas são mais recorrentes e importantes de se estudar. São elas: Hidrocarbonetos, Álcoois, Fenóis, Éteres, Cetonas, Aldeídos, Ácidos Carboxílicos, Ésteres, Aminas, Amidas e Haletos Orgânicos. Veja abaixo:
Hidrocarbonetos
São denominados hidrocarbonetos os compostos orgânicos que possuem somente os átomos de carbono e hidrogênio em sua estrutura, sendo sua fórmula geral a CxHy.
São classificados de acordo com o tipo de ligação (simples, dupla ou tripla) presente entre os átomos de carbono, além do fato de a cadeia ser aberta ou cíclica.
Publicidade
Nomenclatura
A nomenclatura é dada de acordo com a União Internacional de Química Pura e Aplicada (IUPAC):
Exemplos:
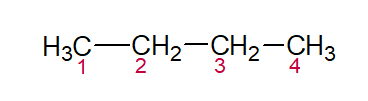
BUT (dos quatro C na cadeia) + AN (das simples ligações) + O (sufixo para hidrocarbonetos) = Butano
Publicidade
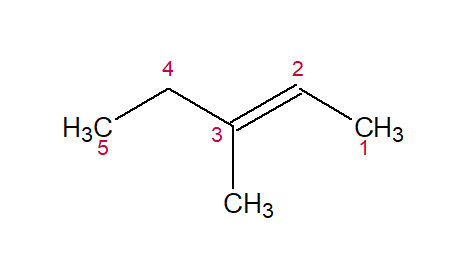
3-METIL (do grupo metil ramificado no carbono 3) + PENT (dos cinco C na cadeia) + 2-EN (da ligação dupla no carbono 2) + O (sufixo para hidrocarbonetos) = 3-metil-pent-2-eno
Álcoois
Os álcoois possuem, em sua estrutura molecular, um ou mais grupos hidroxila (OH) ligados aos átomos de carbono saturado (que realiza somente ligações simples). Esses carbonos, por sua vez, podem estar ligados a uma cadeia carbônica. Por isso, a representação geral de um álcool é dada pelo grupo OH ligado a um substituinte R, indicando a cadeia.
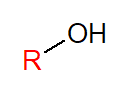
Os álcoois são divididos de acordo com a quantidade de hidroxilas (ou grupos álcoois) presentes na molécula. Um grupo álcool caracteriza um monoálcool, que pode ser primário, secundário ou terciário, de acordo com o tipo de carbono onde se encontra a hidroxila. Quando há dois grupos OH, é chamado de diálcool. Três ou mais, é denominado poliálcool.
Nomenclatura
Os álcoois são nomeados de maneira similar aos hidrocarbonetos, substituindo o sufixo O por OL. Deve-se começar a contagem dos carbonos partindo da extremidade da cadeia mais próxima ao grupo -OH e também indicar, de acordo com o número do carbono, a posição do grupo álcool presente.
Exemplos:
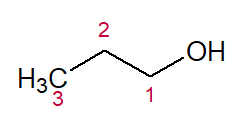
PROP (dos três C na cadeia) + AN (das simples ligações) + 1-OL (posição da hidroxila e sufixo para álcoois) = Propan-1-ol
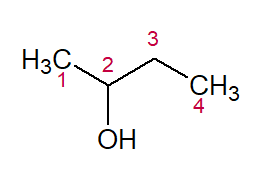
BUT (dos três C na cadeia) + AN (das simples ligações) + 2-OL (posição da hidroxila e sufixo para álcoois) = Butan-2-ol
Fenóis
Fenóis são constituídos de um ou mais grupo hidroxila (OH) ligado diretamente a um anel aromático, fato que faz com que sejam diferentes dos álcoois comuns. São classificados de acordo com a quantidade de hidroxilas ligadas ao anel, sendo monofenol (1 OH), difenol (2 OH) ou polifenol (3 ou mais OH).
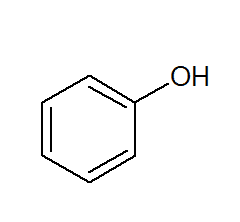
Nomenclatura
Há várias maneiras de se nomear os fenóis, todas partindo do pressuposto de que o anel aromático é a cadeia principal na hora de numerar os carbonos, onde se encontram os substituintes. A mais simples delas é adicionar o radical correspondente ao substituinte antes da palavra fenol.
Exemplos:
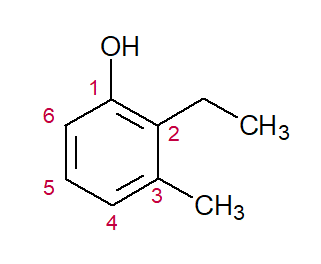
2-ETIL (posição e nome do substituinte em ordem alfabética) + 3-METIL (posição e nome do segundo substituinte) + fenol (nomenclatura da classe) = 2-etil-3-metil-fenol
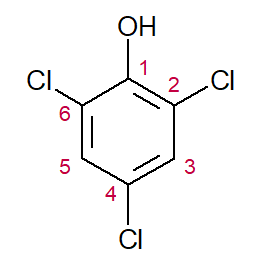
2,4,6-tricloro (posições e nome do substituinte) + fenol (nomenclatura da classe) = 2,4,6-tricloro-fenol
Éteres
Os éteres são constituídos por moléculas onde um átomo de oxigênio se encontra ligado entre duas cadeias carbônicas. Eles podem ser simétricos, quando as duas cadeias substituintes forem iguais, ou assimétricos, quando forem diferentes.
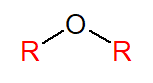
Nomenclatura
De acordo com a IUPAC, a nomenclatura dos éteres é feita separando os dois radicais da molécula em simples (menor número de carbonos) e complexo (maior número de C). Sendo assim, o nome do éter segue a estrutura:
Radical mais simples + OXI (referente aos éteres) + radical complexo + terminação de hidrocarbonetos
Quando for um éter simétrico, é só adicionar a palavra ÉTER antes do nome do radical.
Exemplos:
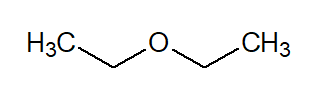
ÉTER (referente à função) + ETIL (referente aos radicais do éter simétrico) + ICO (referente à terminação do radical) = Éter etílico
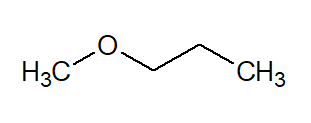
MET (do radical mais simples) + OXI (referente aos éteres) + PROP (do radical mais complexo) + AN (das simples ligações) + O (terminação de hidrocarboneto) = Metóxi propano
Cetonas
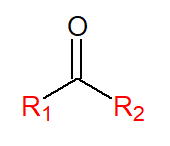
As cetonas são constituídas de uma carbonila (C=O) secundária, ou seja, ligada a dois substituintes orgânicos (R1 e R2). Elas podem ser, assim como os éteres, simétricas ou assimétricas, dependendo dos grupos R1 e R2. Esses dois grupos podem, ainda, estar unidos entre si, fazendo com que a cetona seja cíclica.
Nomenclatura
A nomenclatura das cetonas, segundo a IUPAC, é feita apenas trocando o sufixo -o dos hidrocarbonetos por -ona. As cetonas podem também ser nomeadas de acordo com os radicais que estão ligados à carbonila. Primeiramente, por ordem crescente dos números de carbonos, são colocados os radicais correspondentes, terminando com a palavra “cetona”, mas essa forma não é a oficial.
Exemplos:
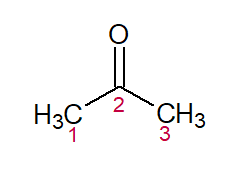
PROP (dos três C na cadeia) + AN (das simples ligações) + ONA (sufixo para cetonas) = Propanona ou dimetil-cetona
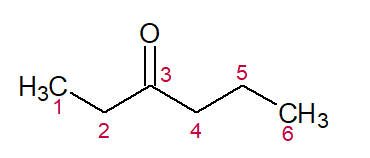
HEX (dos seis C na cadeia) + AN (das simples ligações) + 3-ONA (sufixo para cetonas, indicando o número do carbono em que se encontra) = Hexan-3-ona ou metil-propil-cetona
Aldeídos
Aldeído é a classe de compostos orgânicos que possuem uma carbonila (C=O) no fim da cadeia carbônica, como representado abaixo, fazendo com que o C da carbonila seja um carbono primário (de um lado, há a cadeia carbônica e, de outro, um átomo de hidrogênio).
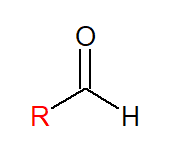
Nomenclatura
Os aldeídos são nomeados de modo parecido ao dos álcoois, substituindo a terminação O dos hidrocarbonetos, desta vez, por AL. A contagem dos carbonos começa a partir do grupo funcional. Apesar disso, muitos são conhecidos por seus nomes usuais, como é o caso do formol (metanal).
Exemplos:
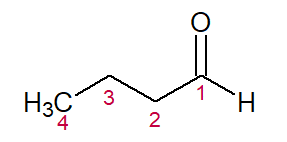
BUT (dos quatro C na cadeia) + AN (das simples ligações) + AL (sufixo para aldeídos) = Butanal
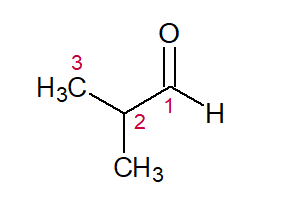
2-METIL (do substituinte da posição 2) + PROP (dos três C na cadeia) + AN (das simples ligações) + AL (sufixo para aldeídos) = 2-metil-propanal
Ácidos Carboxílicos
Os ácidos carboxílicos são compostos orgânicos que possuem em sua estrutura uma (ou mais) carboxila (RCOOH) ligada à cadeia carbônica.
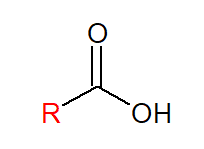
O hidrogênio do grupo carboxila é levemente ácido, dando a característica dos compostos dessa classe do pH um pouco menor do que 7.
Nomenclatura
Para nomear os ácidos carboxílicos, é facil: começamos com a palavra “ácido”, seguido pelo nome correspondente ao número de carbonos da cadeia que forma a molécula, pelo tipo de ligação da mesma maneira dos hidrocarbonetos e pela terminação OICO, característica dessa classe.
Exemplos:
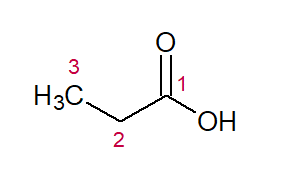
ÁCIDO (referente à função) + PROP (dos quatro C na cadeia) + AN (das simples ligações) + OICO (sufixo para ácidos carboxílicos) = Ácido Propanoico
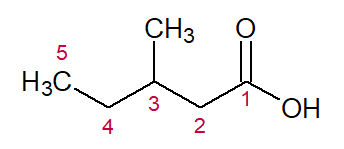
ÁCIDO (referente à função) + 3-METIL (do substituinte da posição 3) + PENT (dos três C na cadeia) + AN (das simples ligações) + OICO (sufixo para ácidos carboxílicos) = Ácido 3-metil-pentanoico
Ésteres
Os ésteres são o conjunto de compostos que possuem, no meio de sua estrutura, uma carbonila substituída por uma cadeia carbônica de um lado (R) e um oxigênio ligado a outra cadeia carbônica do outro, como representado abaixo:
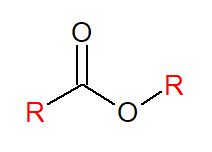
Nomenclatura
É formada por um prefixo que indica o número de carbonos do radical da extremidade e não possui o oxigênio (o carbono da carbonila entra na contagem) + um intermediário (indicador do tipo da ligação química existente nesse radical) + sufixo oato de (característico dos ésteres) + o mesmo para o segundo radical + sufixo ila.
Exemplos:
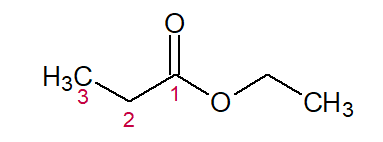
PROP (dos três C na cadeia) + AN (das simples ligações) + OATO (sufixo para ésteres) + de + ET (da outra cadeia) + ILA = Propanoato de etila
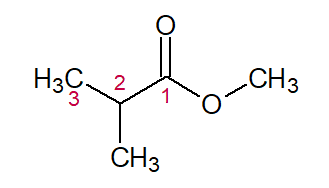
2-METIL (do substituinte na posição 2) + PROP (dos três C na cadeia) + AN (das simples ligações) + OATO (sufixo para ésteres) + de + MET (da outra cadeia) + ILA = 2-metil-propanoato de metila
Aminas
Aminas são compostos orgânicos derivados da amônia (NH3). Eles surgem quando os hidrogênios são substituídos por cadeias orgânicas.
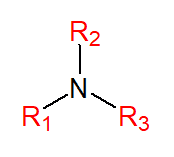
As aminas podem ser primárias – quando ligadas a apenas um substituinte e dois átomos de hidrogênio -, secundárias ou terciárias (dois e três substituintes, respectivamente).
Nomenclatura
A nomenclatura é feita com o nome do substituinte primeiro, seguido da terminação amina. Quando essa for secundária ou terciária, a posição do substituinte que também se encontra ligado ao nitrogênio é indicada pela letra N.
Exemplos:
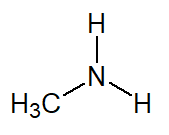
MET (do substituinte com um átomo de C) + IL (terminação do radical) + AMINA (terminação da classe) = Metilamina
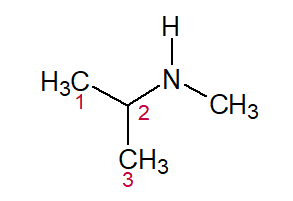
N-METIL (do substituinte com um átomo de C de um lado do nitrogênio) + PROP (dos 3 C na cadeia) + AN (das ligações simples) + 2-AMINA (terminação da classe com a indicação de qual carbono está ligada na cadeia carbônica) = N-metil-propan-2-amina
Amidas
Também são compostos orgânicos derivados da amônia, estruturalmente semelhantes aos ácidos carboxílicos, se diferenciando pela substituição da hidroxila (OH) pelo grupamento amino (NH2)
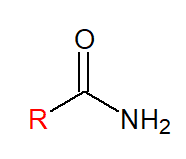
Nomenclatura
A nomenclatura parte do principio dos hidrocarbonetos, adicionando a palavra “amida” ao fim.
Exemplos:
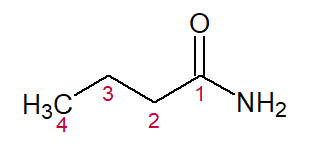
BUTANO (nome do hidrocarboneto correspondente) + AMIDA (representando o grupo funcional) = Butanoamida
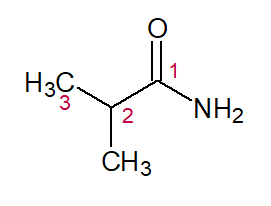
2-METIL (referente ao substituinte no carbono 2) + PROPANO (nome do hidrocarboneto correspondente) + AMIDA (representando o grupo funcional) = 2-metil-propanoamida
Haletos Orgânicos
São funções que possuem em sua estrutura um halogênio (flúor, cloro, bromo ou iodo).
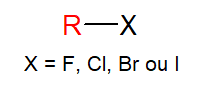
Haletos orgânicos são compostos formados pela substituição de um átomo de hidrogênio de um hidrocarboneto por um átomo de halogênio. Geralmente são tóxicos e danosos para os seres vivos.
Nomenclatura
É dada pelo nome do halogênio substituinte seguido do hidrocarboneto correspondente à cadeia carbônica.
Exemplos:
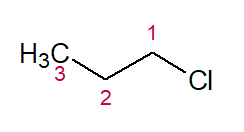
CLORO (do halogênio) + PROPANO (do hidrocarboneto) = Cloro-propano
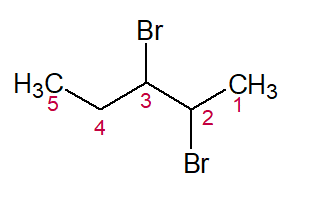
2,3-DIBROMO (dos dois halogênios nas posições 2 e 3 da cadeia carbônica) + PENTANO (do hidrocarboneto) = 2,3-dibromo-pentano
Vídeos sobre as funções orgânicas
Que tal conferir agora alguns vídeos sobre a matéria para conhecer melhor as funções orgânicas? Acompanhe abaixo:
Revisão – funções orgânicas
Nesse vídeo, você acompanha uma revisão sobre as funções vistas anteriormente de uma maneira mais prática, para reconhecer e diferenciar cada uma delas.
Como diferenciar funções orgânicas?
Aqui, você vê como é possível diferenciar as diversas funções que podem existir em uma mesma molécula química.
Exercícios de vestibular sem complicações
Já nesse vídeo, o professor Marcelo explica como resolver exercícios de vestibular sem medo. Vale a pena conferir!
Em química orgânica, existe uma grande variedade de compostos. A maneira encontrada para categorizá-los foi por semelhança – muitas vezes, características físico-químicas -, em que os compostos com uma mesma sequência de átomos em sua estrutura seriam da mesma classe. Que tal aprender um pouco mais sobre as funções oxigenadas, conhecendo os principais compostos de cada uma delas?
Referências
Princípios de química: questionando a vida moderna e o meio ambiente (2012) – Peter W. Atkins e Loretta Jones

Por Lucas Makoto Tanaka dos Santos
Bacharel em Química pela Universidade Estadual de Maringá (UEM), mestrando em Química Analítica, com ênfase em desenvolvimento de métodos analíticos, metabolômica e espectrometria de massas no Laboratório de Biomoléculas e Espectrometria de Massas (LaBioMass), na mesma universidade.
Tanaka dos Santos, Lucas Makoto. Funções orgânicas. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/funcoes-organicas. Acesso em: 06 de May de 2026.
1.
O aspartame (figura) é um adoçante artificial não-sacarídeo cerca de 200 vezes mais doce que a sacarose, o nosso açúcar de mesa.
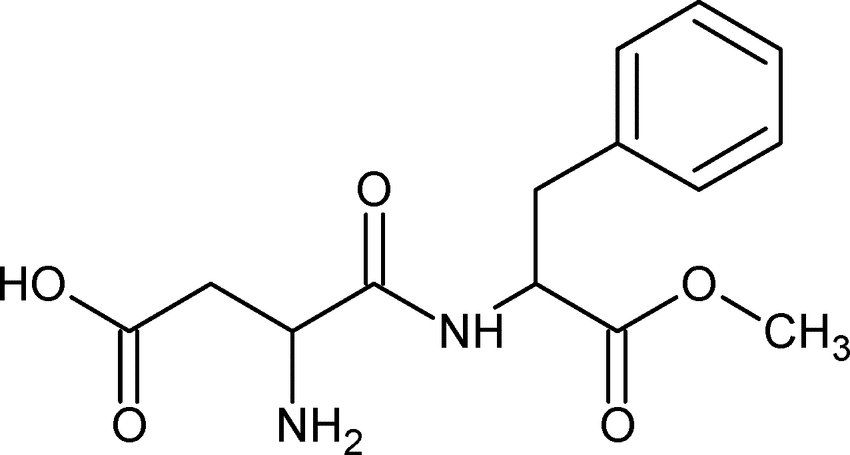
Sua estrutura consiste de diferentes funções orgânicas. Sabendo disso e com o que aprendemos até agora, quais são estas funções?
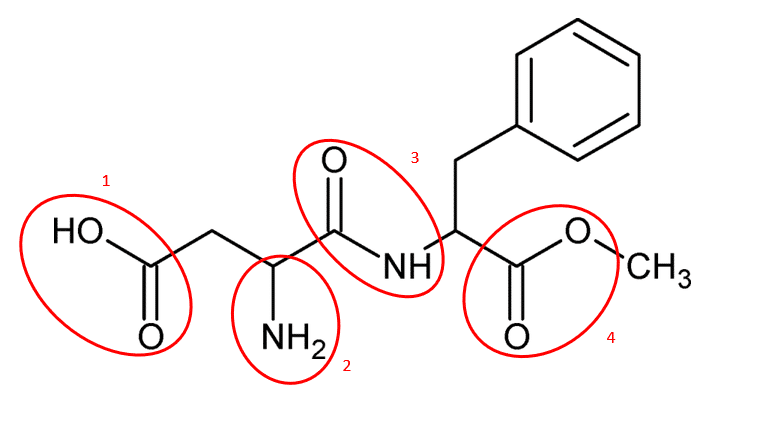
As funções orgânicas existentes são ácido carboxílico (1), amina (2), amida (3) e éster (4).
2. [UNESPAR - 2015]
A nomenclatura dos compostos orgânicos é feita de tal modo que no próprio nome há uma indicação da função à qual a substância pertence. Considere a relação: ácido propanoico, butanal, propanona e butanol. Indique a alternativa que representa a função de cada um dos compostos respectivamente:
A) álcool, aldeído, cetona, ácido carboxílico;
B) ácido carboxílico, aldeído, cetona, álcool;
C) ácido carboxílico, aldeído, álcool, cetona;
D) aldeído, álcool, cetona, ácido carboxílico;
E) cetona, ácido carboxílico, álcool, éter.
Resposta correta:
B) ácido carboxílico, aldeído, cetona, álcool;
3.
Uma substância que pode ser utilizada no tratamento de pneumonia é a cefalexina, cuja estrutura é mostrada a seguir:
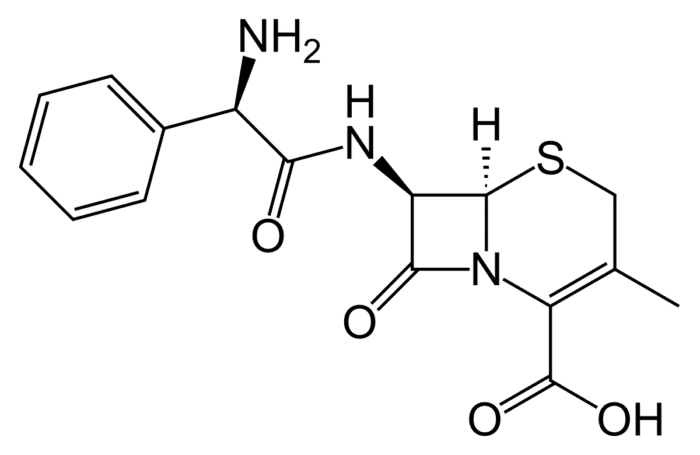
Quais as funções orgânicas, das vistas até agora, que estão presentes na estrutura da cefalexina?
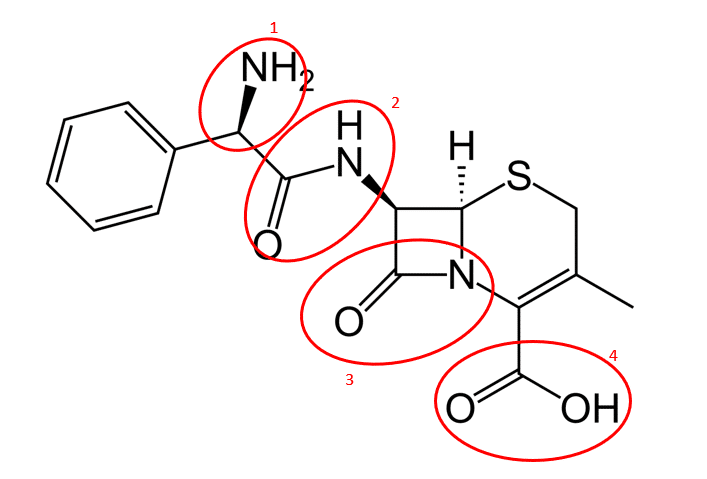
Amina (1), Amida (2 e 3) e ácido carboxílico (4).