O éter é um grupo funcional de compostos orgânicos constituído de moléculas, nas quais um átomo de oxigênio se encontra entre duas cadeias carbônicas. Podem ser simétricos ou assimétricos, conforme a semelhança das cadeias substituintes. Além disso, são compostos utilizados, principalmente, como solventes inertes. Entenda mais sobre essa classe de substâncias e suas características.
Publicidade
O que é o éter
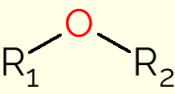
O éter é uma classe de compostos orgânicos que contém um oxigênio ligado a duas cadeias carbônicas (grupos alquil para cadeias abertas, ou aril se a cadeia for um anel aromático). A fórmula genérica desses compostos é R1–O–R2, na qual R1 e R2 representam as cadeias carbônicas. Devido a presença do átomo de oxigênio, as ligações C-O-C das moléculas de éter têm ângulo de 105°. Portanto, são levemente polarizadas pela maior eletronegatividade do oxigênio.
Relacionadas
Os compostos dessa classe são usados principalmente como solventes em reações orgânicas, sendo produzidos geralmente por desidratação de álcoois com ácido sulfúrico. São compostos com odor agradável, que são facilmente volatilizados e que possuem as propriedades conhecidas há muito tempo. Sendo assim, já foram empregados vastamente na história da medicina como anestésicos, principalmente o etoxietano, visto que ele adormece a dor e deixa o paciente consciente.
Características dos éteres
Veja as principais características dos compostos orgânicos da classe dos éteres:
- São líquidos em temperatura ambiente, desde que possuam mais de quatro átomos de carbono na estrutura;
- Geralmente são compostos que apresentam densidade menor que a da água;
- Éteres de menor massa são ligeiramente solúveis em água;
- São compostos polares, visto que apresentam uma geometria angular por conta da presença do átomo de oxigênio;
- As substâncias têm odores característicos e, muitas vezes, agradáveis. Porém, podem causar dependência ou danos à saúde;
- Realiza ligações de hidrogênio com moléculas de água ou álcoois, entretanto, com outras moléculas de éter, fazem interação fraca do tipo dipolo permanente, dada a baixa polaridade dos compostos;
- Comparado à outros compostos orgânicos de massa molar semelhante, os éteres têm pontos de fusão parecidos com os de alcanos, porém menores que os dos demais compostos orgânicos.
Eles ainda possuem a característica de formar polímeros – os conhecidos “poliésteres” – comuns na indústria têxtil. Além disso, os éteres podem ser classificados como simétricos ou não. Entenda isso a seguir.
Tipos de éter
Conforme as cadeias carbônicas que compõem os éteres, eles são classificados como simétricos ou assimétricos.
Publicidade
- Simétrico: é um éter que possui as cadeias de C idênticas, como por exemplo o dimetil éter, etoxietano ou o propoxipropano (com 1, 2 e 3 carbonos nas cadeias carbônicas, respectivamente);
- Assimétrico: ocorre quanto o composto possui as cadeias carbônicas diferentes. É o caso do etoxibenzeno, em que um lado existe o anel aromático e de outro a cadeia com dois átomos de C.
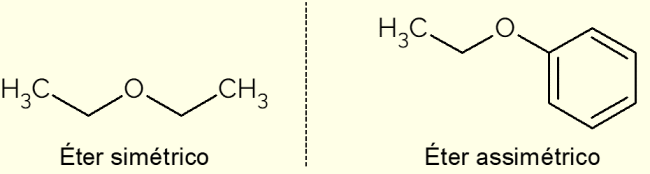
Na imagem acima está a representação do etoxietano e do etoxibenzeno, compostos que ilustram as diferenças entre um éter assimétrico de um simétrico.
Nomenclatura
Conforme a IUPAC, para nomear os compostos da classe éter é necessário dividir a molécula em duas partes, tomando o oxigênio como ponto da divisão. De um lado fica o substituinte mais simples (menor número de carbonos) e, do outro, o mais complexo (maior número de C). Sendo assim, o nome do éter segue a estrutura: MENOR cadeia carbônica + OXI (referente aos éteres) + MAIOR cadeia de C + terminação idêntica a dos hidrocarbonetos.
Um exemplo é o metoxietano (CH3OCH2CH3): MET (da cadeia menor) + OXI (do grupo funcional) + ET (da cadeia maior) + ANO (terminação igual a dos hidrocarbonetos)
Publicidade
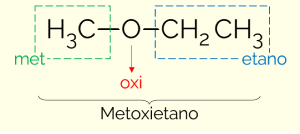
Há uma segunda maneira de nomear os éteres. É um modo mais usual, que consiste em colocar os nomes dos substituintes em ordem alfabética e adicionar a palavra éter ao final. Sendo assim, o exemplo acima também pode ser chamado de “etil metil éter”.
Éteres importantes
Veja alguns éteres que são importantes, devido suas utilidades e características:
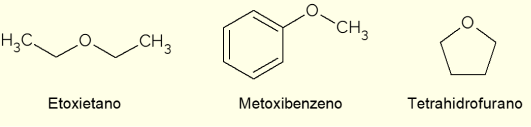
- Etoxietano: é um líquido incolor e de odor adocicado. Tem ponto de ebulição baixo (34,6 °C) e antigamente era usado como anestésico. Hoje em dia é empregado como solvente de extração, como refrigerante de máquinas ou como combustível de ignição de motores à diesel;
- Metoxibenzeno: é um éter arílico, ou seja, apresenta o benzeno na estrutura. É um dos principais componentes do óleo essencial de anis ou erva-doce, portanto está presente em algumas fragrâncias;
- Tetrahidrofurano (THF): é um composto heterocíclico, ou seja, de cadeia fechada com a presença de um átomo de oxigênio. Nesse caso, é um éter cíclico líquido, sem coloração e de baixa viscosidade, usado como solvente inerte em reações químicas ou como precursor na produção de polímeros.
Existem outros éteres importantes, com as mais variadas aplicações e propriedades. Entre eles estão os epóxidos, éteres cíclicos (assim como o THF), usados na produção de resinas epóxi. Apesar disso, a maioria dos éteres são usados como solventes em reações químicas.
Vídeos sobre os éteres
Agora que o conteúdo foi apresentado, veja alguns vídeos selecionados para ajudar a assimilar o tema do estudo de compostos orgânicos oxigenados:
Nomenclatura de compostos da classe dos éteres
Existe mais de uma maneira de realizar a nomenclatura dos compostos com o grupo funcional de éter na estrutura. Sendo assim, é importante ter conhecimento de todas elas, mesmo que a forma tradicional da IUPAC seja a recomendada. Muitas vezes, questões de vestibulares apresentam os compostos com seus nomes comuns. Veja esse vídeo e aprenda como nomear os éteres.
A função orgânica éter
A função orgânica “éter” corresponde aos compostos que apresentam uma ligação de C-O-C no meio da molécula. São compostos de odor adocicado e, geralmente, são utilizados como solventes. Aprenda sobre a importância dessa classe de compostos e uma forma de nomear os éteres pela análise das cadeias que substituem o átomo central de oxigênio.
Resolução de exercícios sobre nomenclatura de éteres
A nomenclatura de éteres é importante e conhecê-la pode ajudar na resolução de exercícios em vestibulares. Sendo assim, veja esse vídeo com exemplos resolvidos sobre a nomenclatura IUPAC de compostos da classe dos éteres. Lembre-se que, em alguns casos, o nome da molécula pode aparecer na sua forma popular, diferente da recomendada pela IUPAC, portanto também é importante saber sobre esta.
Em síntese, os compostos do grupo funcional éter tem como característica a presença de um oxigênio central, com duas cadeias carbônicas ligadas diretamente nele. São utilizados como solventes e podem ser simétricos ou assimétricos. Não pare de estudar por aqui, aprenda sobre outro grupo funcional de nome semelhante, porém com características distintas, os ésteres.
Referências
Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente (2005) – Peter Atkins e Loretta Jones
Química: a ciência central (1999) – Theodore L. Brown, Eugene H. LeMay, Bruce E. Bursten e Julia R. Burdge
Química Orgânica (1976) – T. W. Graham Solomons
Ether and Chloroform (On-line) – Disponível em: https://www.history.com/topics/inventions/ether-and-chloroform. Acesso em 06 de dez. de 2021.

Por Lucas Makoto Tanaka dos Santos
Bacharel em Química pela Universidade Estadual de Maringá (UEM), mestrando em Química Analítica, com ênfase em desenvolvimento de métodos analíticos, metabolômica e espectrometria de massas no Laboratório de Biomoléculas e Espectrometria de Massas (LaBioMass), na mesma universidade.
Tanaka dos Santos, Lucas Makoto. Éter. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/eter. Acesso em: 06 de May de 2026.
1. [Cesgranrio]
Quantos éteres acíclicos diferentes têm fórmula molecular C4H10O?
a) 1
b) 2
c) 3
d) 4
e) 5
O éter acíclico é aquele de cadeia aberta. Realizando a montagem das estruturas possíveis com a fórmula C4H10O, tem-se:

Sendo assim, a alternativa correta é a letra c) 3.
2. [UFRN]
O etoxietano (éter comum), usado como anestésico em 1842, foi substituído gradativamente por outros anestésicos em procedimentos cirúrgicos. Atualmente, é muito usado como solvente apolar nas indústrias, em processos de extração de óleos, gorduras, essências, entre outros. A estrutura do éter comum que explica o uso atual mencionado no texto é:
a) CH3–CH2–CH2–CH2–OH.
b) CH3–CH2–O–CH2–CH3.
c) CH3–CH2–CH2–CH–O.
d) CH3–CH2–CH2–CO2H.
e) CH3–O–CH2–CH2–CH3.
O etoxietano é um éter simétrico com as cadeias carbônicass que possuem dois átomos de carbono em cada. Sendo assim, a alternativa correta é a letra b) CH3–CH2–O–CH2–CH3.