A matéria, de maneira geral, é definida como tudo o que ocupa lugar no espaço e possui massa. As propriedades da matéria são fundamentais para a química, uma vez que permitem identificar diferentes compostos. Elas podem ser divididas em dois grupos: gerais e específicas, as quais serão apresentadas a seguir. Confira!
Publicidade
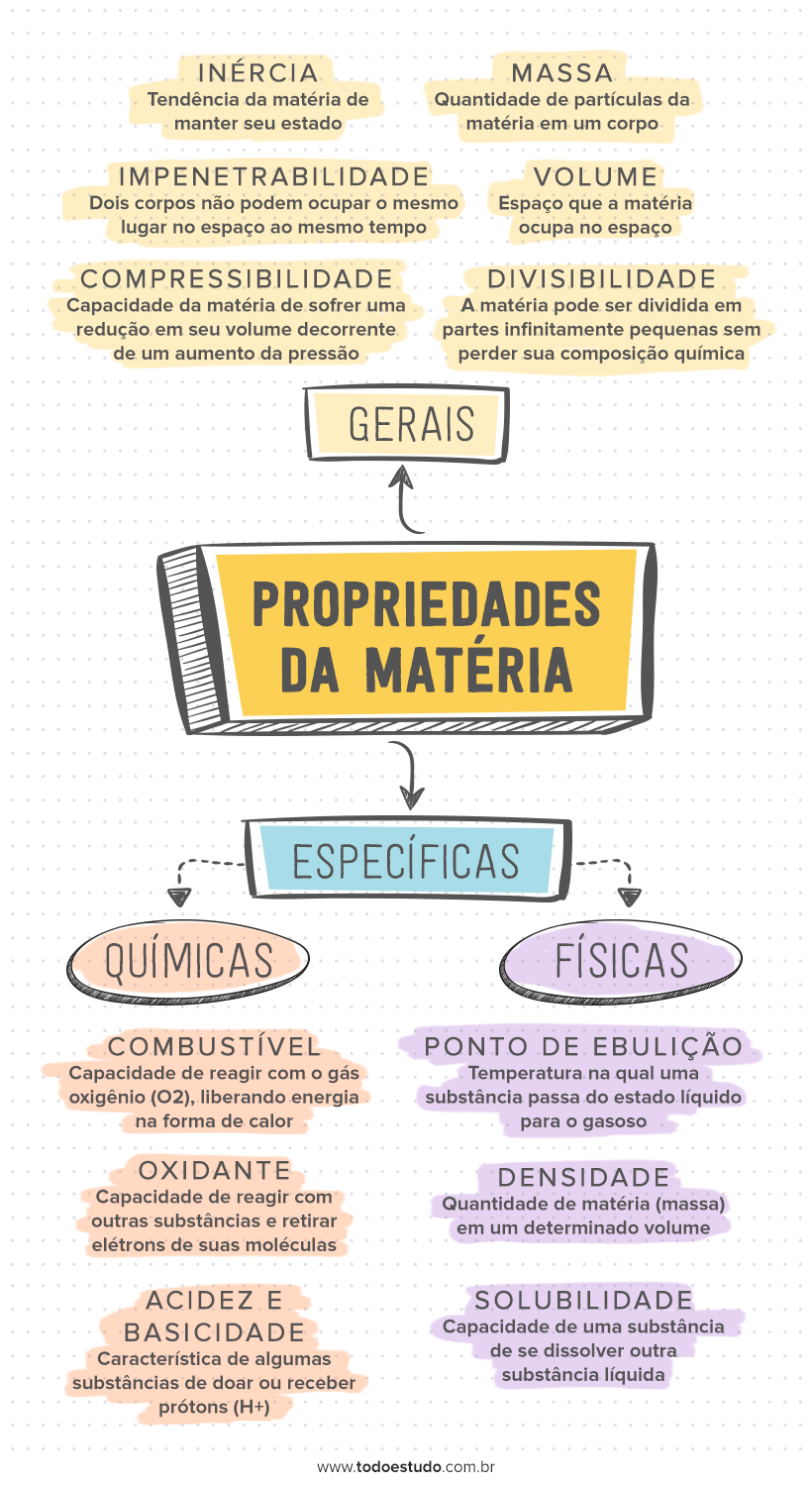
Propriedades gerais da matéria
As propriedades gerais são aquelas que se aplicam a toda matéria, independente de como ela é constituída e de seu estado físico – seja sólido, líquido ou gasoso. É possível citar algumas importantes e mais utilizadas no contexto químico, que são estas apresentadas abaixo.
Relacionadas
Inércia
Corresponde à tendência da matéria de manter seu estado, seja em repouso ou em movimento, a não ser que haja a ação de uma força externa sobre ela. Então, um corpo tende a permanecer parado e só mudará seu estado caso sofra a ação da força externa, por exemplo.
Massa
A massa corresponde à quantidade de partículas da matéria em um corpo. Ou seja, é a grandeza mensurável que nos dá a noção de quão pesado ou leve algum objeto é. Portanto, a unidade de medida da massa é, no Sistema Internacional de Unidades (SI), o quilograma (kg).
Volume
Diz respeito ao espaço que a matéria ocupa no espaço, em qualquer um dos estados físicos em que ela possa se apresentar. Sendo assim, no SI, o volume é medido em metros cúbicos (m3), porém no cotidiano é utilizado o litro (L).
Impenetrabilidade
Corresponde ao fato de que dois corpos não podem ocupar o mesmo lugar no espaço ao mesmo tempo.
Publicidade
Compressibilidade
A compressibilidade é a capacidade da matéria de sofrer uma redução em seu volume, decorrente de um aumento da pressão que atua sobre ela. Todas as substâncias sofrem essa compressão, porém algumas em maior extensão, como é o caso dos gases.
Divisibilidade
A matéria pode ser dividida em partes infinitamente pequenas sem perder sua composição química.
Dessa maneira, como as propriedades gerais se aplicam a toda matéria, não é possível identificar uma substância apenas ao determinar sua massa ou seu volume, por exemplo. Para tal, fazemos o uso das propriedades específicas que veremos a seguir.
Publicidade
Propriedades específicas da matéria
Quando falamos de propriedade específica da matéria, falamos das características intrínsecas de uma substância, que permitem identificar e diferenciar dois compostos diferentes. Ou seja, elas são exclusivas de determinada substância. São divididas em químicas e físicas. Veja abaixo:
Químicas
As propriedades químicas são aquelas correspondentes à capacidade da matéria de sofrer um processo de transformação ou reação química, mesmo que esse dependa de condições reacionais determinadas.
- Combustível: é a capacidade de reagir com o gás oxigênio (O2), liberando energia na forma de calor.
- Oxidante: é a capacidade de reagir com outras substâncias e retirar elétrons de suas moléculas.
- Acidez e basicidade: correspondem à característica de algumas substâncias de doar ou receber prótons (H+), alterando o pH de uma solução, por exemplo.
Físicas
As propriedades físicas são inerentes da matéria, ou seja, elas não dependem de transformações que ocorrem.
- Ponto de fusão: é a temperatura na qual uma substância passa do estado físico líquido para o sólido, ou o contrário.
- Ponto de ebulição: temperatura na qual uma substância passa do estado líquido para o gasoso.
- Densidade: é a quantidade de matéria (massa) em um determinado volume. Portanto, é determinada pela razão entre massa e volume (m/V).
- Solubilidade: é a capacidade de uma substância de se dissolver em outra substância líquida.
Como vimos, as propriedades químicas dependem das transformações que ocorrem em uma reação química. Já as físicas são intrínsecas da própria matéria. Dessa forma, as propriedades da matéria são muito úteis na identificação de diferentes substâncias.
Além dessas, existem as propriedades organolépticas, que garantem as características perceptíveis aos nossos sentidos, como odor e aparência.
Vídeos sobre as propriedades da matéria
Agora, que tal ver alguns vídeos que te ajudarão a compreender a matéria e suas propriedades? Acompanhe a selação abaixo:
Propriedades gerais da matéria
Nessa animação, compreendemos melhor algumas das propriedades gerais da matéria. Ou seja, aquelas que são comuns a todo corpo e não diferenciam um do outro.
Relação entre matéria e estado físico
Aqui, além de entendermos melhor o conceito de matéria, vemos também como ela se relaciona com os estados físicos (sólido, líquido e gasoso).
As propriedades específicas
Esse vídeo é focado em explicar sobre as propriedades específicas da matéria, ou seja, as propriedades físicas e químicas.
Em conclusão, a compreensão das diferentes propriedades da matéria é muito útil na química, pois ajuda a predizer o comportamento da mistura de duas substâncias e saber o rumo que uma reação química poderá tomar, evitando possíveis acidentes. Não pare seus estudos aqui: leia também sobre dois processos que envolvem as propriedades da matéria, a liquefação e a vaporização.
Referências
HALLIDAY, David; RESNICK, Robert; WALKER, Jearl. Fundamentos de Física, vol. 2: Mecânica. 8ª edição. 2008.
ATKINS, P.W., Jones, L. Princípios de química: questionando a vida moderna e o meio ambiente. 5ª edição. Porto Alegre: Ed. Bookman, 2012.

Por Lucas Makoto Tanaka dos Santos
Bacharel em Química pela Universidade Estadual de Maringá (UEM), mestrando em Química Analítica, com ênfase em desenvolvimento de métodos analíticos, metabolômica e espectrometria de massas no Laboratório de Biomoléculas e Espectrometria de Massas (LaBioMass), na mesma universidade.
Tanaka dos Santos, Lucas Makoto. Propriedades da matéria. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/propriedades-da-materia. Acesso em: 07 de May de 2026.
1.
Indique as afirmações abaixo em propriedade geral (G), química (Q) ou física (F) e correlacione com a alternativa correta.
( ) O ferro enferruja na presença de ar e umidade.
( ) Em temperatura ambiente, o ferro é sólido e de cor cinza.
( ) Quando o papel pega fogo, ocorre a produção de cinzas..
( ) A densidade da água é de aproximadamente 1 g/cm3
( ) A água ferve à temperatura de 100ºC, em pressão atmosférica de 1 atm.
( ) A combustão da gasolina libera gases e energia térmica.
A alternativa correspondente às propriedades é:
A ) G – F – F – G – Q – Q
B ) Q – G – Q – G – Q – F
C ) Q – G – Q – F – F – Q
D ) Q – G – G – Q – F – F
E ) F – G – F – Q – F – Q
– O ferro enferruja por conta de sua oxidação, um fenômeno químico;
– Essas características não distinguem o ferro de algum outro sólido cinza, portanto é uma propriedade geral;
– A combustão do papel é uma propriedade química;
– A densidade é uma propriedade física;
– A temperatura de fervura da água é também seu ponto de ebulição, uma característica física;
– Combustão = propriedade química.
Portanto, a alternativa correta é a letra C ) Q – G – Q – F – F – Q.
2. [(UNB-DF) adaptada]
Julgue os itens abaixo, indicando aqueles que se referem a propriedades químicas das substâncias e aqueles que se referem a propriedades físicas das substâncias.
1) O etanol entra em ebulição a 78,5°C.
2) O éter etílico sofre combustão.
3) O sódio metálico é um sólido mole e de baixo ponto de fusão.
4) O metabolismo do açúcar no corpo humano leva à produção de dióxido de carbono e água.
1) Física
2) Química
3) Física
4) Química
3. [(PUC-MG) ]
Em um laboratório de química, foram encontrados cinco recipientes sem rótulo, cada um contendo uma substância pura líquida e incolor. Para cada uma dessas substâncias, um estudante determinou as seguintes propriedades:
1. Ponto de ebulição
2. Massa
3. Volume
4. Densidade
Assinale as propriedades que podem permitir ao estudante a identificação desses líquidos.
a) 1 e 2
b) 1 e 3
c) 2 e 4
d) 1 e 4
Alternativa d) 1 e 4, ponto de ebulição e densidade, que são propriedades específicas. Massa e volume são propriedades gerais e comuns a todas as substâncias.