A eletrosfera é a região no átomo que agrega as partículas de carga negativa, ou seja, os elétrons. É um conceito introduzido com o modelo atômico de Rutherford que, a partir de experimentos, percebeu uma região de cargas opostas ao redor do núcleo do átomo. Aprenda o que é a eletrosfera, e sua organização.
Publicidade
O que é a eletrosfera
Um átomo é constituído de um núcleo, onde se encontram as partículas carregadas positivamente (prótons) e as de carga nula (nêutrons). E de uma camada externa, onde ficam localizados os elétrons, partículas de carga negativas. Essa região negativamente carregada é chamada de eletrosfera.
Relacionadas
Em seu famoso experimento para explicar o desvio de partículas alfas em emissões radioativas em uma lâmina de ouro, Rutherford constatou que o átomo poderia ser constituído de um núcleo, que representa majoritariamente a massa atômica, e uma camada externa carregada com cargas opostas que neutralizam a carga do átomo. Isso derruba o modelo até então existente, o de Thomson.
Dessa forma, o conceito de eletrosfera passa a ser conhecido. É a região no espaço atômico onde os elétrons se encontram, girando em órbitas circulares de modo semelhante ao sistema solar. Essa região está organizada em níveis energéticos, conhecidos como camadas eletrônicas. Vamos ver como se dá a organização da eletrosfera?
Camadas e organização
A eletrosfera, também chamada de nuvem eletrônica, é dividida em sete camadas energéticas que recebem as letras K, L, M, N, O, P e Q, sendo que a primeira é de menor energia e mais próxima do núcleo, e a última é a mais energética e mais distante do núcleo atômico.
O físico dinamarquês Niels Bohr determinou que os elétrons podem orbitar o núcleo nessas camadas eletrônicas sem ganhar nem perder energia. Porém, se os elétrons saltam para uma camada mais externa, os átomos passam para um estado excitado de energia. Ao voltar para a camada de origem, os elétrons emitem a energia acumulada na forma de fótons, que liberam energia luminosa.
Publicidade

Ainda sobre as camadas eletrônicas, cada uma delas pode comportar uma quantidade limitada de partículas negativas, ou seja, em cada uma, o número de elétrons já é determinado.
Vídeos sobre a eletrosfera
Agora que tem conhecimento sobre o tema, veja alguns vídeos que ajudam a assimilar o conteúdo estudado.
Publicidade
Entendendo as camadas de energia da eletrosfera
Uma parte importante da estrutura atômica é a eletrosfera. Nela encontramos os elétrons de um átomo, e também representa a maior parte do volume atômico. Entenda, nesse vídeo, como a eletrosfera é dividida, conforme os níveis de energia e a quantidade de elétrons que podem estar localizados em cada uma das sete camadas.
A localização dos elétrons em um átomo
Em um átomo, os elétrons estão localizados na região conhecida como eletrosfera. Esta é dividida em camadas e subníveis de energia. Tendo conhecimento dessa organização, é possível descrever um átomo eletronicamente, ou seja, pela configuração dos elétrons. Veja mais sobre a distribuição eletrônica e a eletrosfera com esse vídeo.
A relação entre a eletrosfera com a estrutura atômica
O átomo é constituído por duas partes principais: o núcleo e a eletrosfera. No núcleo se encontram os prótons e os nêutrons. Por outro lado, na eletrosfera se encontram os elétrons. Com esse vídeo, saiba como cada uma dessas partes é descrita. Além disso, tenha um entendimento profundo sobre as divisões e distribuição dos elétrons na eletrosfera de um átomo.
Em síntese, a eletrosfera é a região no átomo que se localizam as partículas de carga negativa, chamadas de elétrons. É dividida em sete camadas, representadas pelas letras de K a Q, em ordem alfabética, conforme os níveis de energia. Não pare de estudar por aqui, aprenda também sobre os números quânticos, que também ajudam a descrever os átomos.
Referências
Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente (2005) – Peter Atkins e Loretta Jones
Química: a ciência central (1999) – Theodore L. Brown, Eugene H. LeMay, Bruce E. Bursten e Julia R. Burdge
Química Inorgânica(1992) – Peter Atkins, Duward F. Shriver e Cooper H. Langford

Por Lucas Makoto Tanaka dos Santos
Bacharel em Química pela Universidade Estadual de Maringá (UEM), mestrando em Química Analítica, com ênfase em desenvolvimento de métodos analíticos, metabolômica e espectrometria de massas no Laboratório de Biomoléculas e Espectrometria de Massas (LaBioMass), na mesma universidade.
Tanaka dos Santos, Lucas Makoto. Eletrosfera. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/eletrosfera. Acesso em: 05 de May de 2026.
1. [ESPM-SP]
O átomo de Rutherford (1911) foi comparado ao sistema planetário (o núcleo atômico representa o sol e a eletrosfera, os planetas):
Eletrosfera é a região do átomo que:
a) contém as partículas de carga elétrica negativa.
b) contém as partículas de carga elétrica positiva.
c) contém nêutrons.
d) concentra praticamente toda a massa do átomo.
e) contém prótons e nêutrons.
Na eletrosfera se encontram os elétrons de um átomo. Os elétrons são as entidades que possuem carga elétrica negativa, ao contrário dos prótons, que têm carga positiva, e dos nêutrons, que têm carga 0 (zero). Dessa forma, a alternativa correta é a letra a) contém partículas de carga elétrica negativa.
2. [EAM - 2012]
Sabe-se que “(…) a ideia de órbitas definidas para os elétrons não é mais aceita; entretanto, o modelo atômico de Rutherford-Bohr continua sendo útil, pois permite a identificação dos elétrons, informa sobre sua distribuição na eletrosfera e facilita a visualização das interações entre os átomos. (…) Nesse modelo, os níveis de energia são representados como anéis concêntricos ao núcleo, as camadas eletrônicas ou níveis de energia. (…) Cada uma das camadas eletrônicas comporta um número máximo de elétrons.”
(CRUZ, Daniel. Tudo é ciência: 9º ano. 2. ed. São Paulo: Ática, 2007, p. 215.)
Observe a tabela abaixo
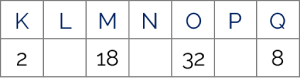
Assinale a opção que possui os números de elétrons que completam corretamente as lacunas na ordem apresentada na tabela.
a) 8, 32, 18
b) 8, 18, 8
c) 18, 32, 18
d) 8, 32, 32
e) 18, 32, 8
As camadas L, N e P, respectivamente, podem comportar no máximo 8, 32 e 18 elétrons (alternativa a).