As reações orgânicas acontecem entre diferentes compostos orgânicos. Existem diferentes tipos de reação, que variam conforme os reagentes e as condições que ocorrem. Indispensável na indústria, essas reações são o principal modo de obtenção de cosméticos, medicamentos e plásticos, por exemplo. Aprenda quais as principais categorias de reações orgânicas e suas características.
Publicidade
O que são reações orgânicas
Quando dois compostos orgânicos reagem entre si, formando ligações novas e, consequentemente, compostos inéditos, dizemos que o tipo de reação que aconteceu foi uma reação orgânica. Além disso, ela pode ocorrer quando uma molécula, em determinada condição, se quebra em duas ou quando há a eliminação de uma molécula menor, como a água.
Relacionadas
Tipos de reações orgânicas
Existem vários tipos de reações orgânicas, mas os quatro principais são as reações de substituição, adição, eliminação e oxidação. Vamos ver, a seguir, o que caracteriza cada um desses tipos de reação, bem como suas subdivisões e especificidades.
Reações orgânicas de substituição
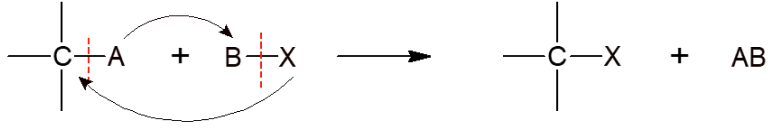
Uma reação de substituição ocorre entre dois compostos diferentes. Nela acontece a troca de um grupo de uma molécula com o grupo, ou átomo, de outro reagente. Ou seja, eles são substituídos entre si. Ela ocorre principalmente com moléculas da classe dos alcanos (lineares ou cíclicos) e anéis aromáticos. Dependendo do grupo que é inserido no primeiro reagente, a reação recebe um nome específico.
Halogenação
Na halogenação, acontece a reação de um alcano com uma molécula diatômica constituída por dois átomos de halogênio, sendo essa a origem do nome, ou seja, acontece a inserção de um halogênio (F, Cl, Br ou I) no alcano. Na imagem abaixo, um exemplo dessa reação, em que o metano (CH4) reage com o gás cloro (Cl2) sob ação de luz ou calor, formando um haleto e o ácido clorídrico.
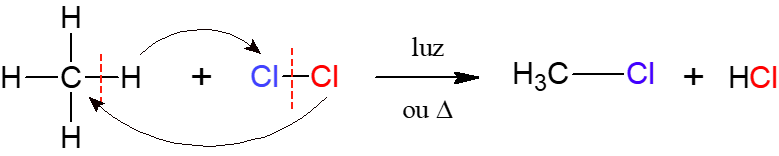
Nitração
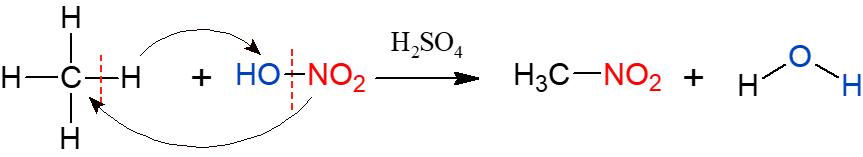
A nitração é semelhante à halogenação, porém dessa vez, o grupo que é substituído e inserido no alcano é um grupo nitro (NO2), proveniente do ácido nítrico (HNO3, representado por HO-NO2 para facilitar a visualização da reação). A reação precisa ser catalisada por ácido sulfúrico. Os produtos dessa reação são um nitrocomposto e água.
Publicidade
Sulfonação
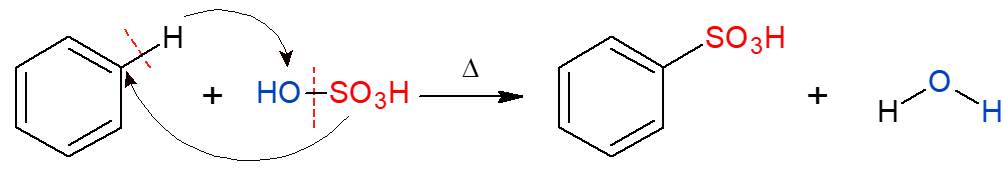
De maneira análoga às vistas anteriormente, na reação de sulfonação ocorre a substituição por um grupo sulfônico (HSO3) no alcano. Na imagem está representada a reação de sulfonação em um anel aromático, que também ocorre, ao reagir o benzeno com o ácido sulfúrico (H2SO4, representado por OH-SO3H), formando como produto um ácido sulfônico e água.
Reações orgânicas de adição
Essa outra classe de reações orgânicas engloba as reações em que dois reagentes formam apenas um produto, já que ocorreu a adição, ou seja, a junção de um deles na outra molécula. Ela ocorre principalmente com alcenos ou alcinos, em outras palavras, moléculas insaturadas, de cadeia aberta. A ligação π se rompe, permitindo a adição dos outros grupos. Conforme o composto que é adicionado, a reação recebe um nome específico.
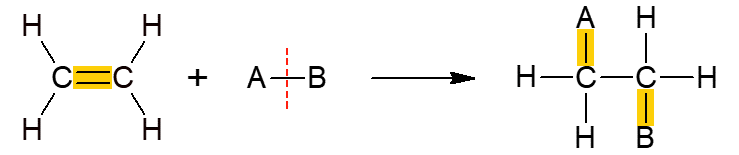
Adição de hidrácidos
Nessa reação, compostos ácidos que contêm hidrogênio, porém não possuem oxigênio, são adicionados ao alceno. É o caso de ácidos como o HCl (clorídrico), HF (fluorídrico) e HCN (cianídrico), por exemplo.
Publicidade
Hidrogenação catalítica
Essa reação é muito usada na indústria alimentícia em processos para fabricação de gordura hidrogenada (gordura trans). Consiste na adição de hidrogênio após a quebra da insaturação de um alceno. A reação produz um alcano e só ocorre sob condições de alta temperatura e pressão, além de um catalisador, por isso o nome “catalítica”.
Halogenação
Nessa reação, acontece a adição de halogênios (F, Cl, Br ou I) ao alceno. É uma reação que tem como produto um di-haleto vicinal, porque os dois átomos da molécula de X2 são adicionados após a quebra da ligação π.
Hidratação
Como o próprio nome já diz, aqui acontece a adição de água à molécula do alceno. Porém, a água é adicionada aos pedaços, ou seja, um H é adicionado a um carbono e o OH em outro. A reação forma um álcool e ocorre em condições ácidas (H3O+).
Todos os subtipos de reações de adição possuem um mecanismo geral semelhante, por isso, todas estão representadas abaixo.
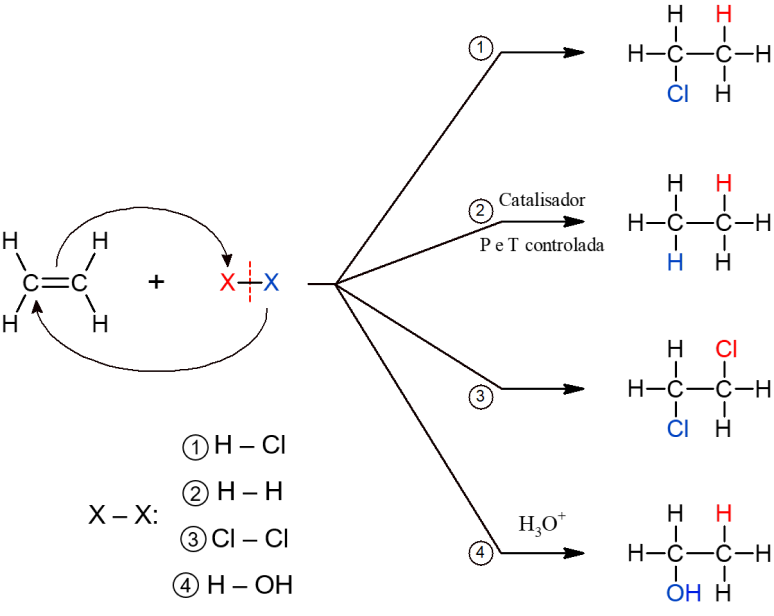
Reações orgânicas de eliminação
A reação de eliminação é o oposto da reação de adição. Nela ocorre a perda de uma molécula menor, oriunda de um alcano, sendo este um dos produtos formados. O segundo produto é um alceno, que surge a partir da reorganização dos elétrons e das ligações químicas depois da perda da molécula.
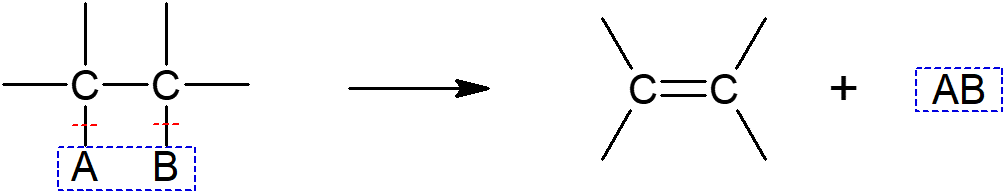
Desidrogenação
Como o próprio nome diz, nessa reação acontece a perda de hidrogênios. Mais precisamente, de uma molécula de H2. É uma reação que acontece somente em condições de aquecimento, ou seja, com o calor como catalisador. O alcano passa a ser um alceno e o segundo produto é o gás hidrogênio.
Desalogenação
Ocorre a perda de dois halogênios da molécula de di-haleto vicinal. É uma reação que, dependendo do halogênio, precisa de catalisadores específicos, como zinco e álcool, por exemplo. Além do alceno, ocorre a formação da molécula diatômica dos halogênios que foram eliminados.
Eliminação de halogenidreto
Também chamada de desidro-halogenação, ocorre a eliminação de um composto constituído de um hidrogênio ligado a um halogênio. Para ela acontecer, é necessária uma catálise alcoólica básica, portanto a reação deve ser levada em uma solução de base forte preparada em meio alcoólico (KOH+Álcool). Quando há mais de dois carbonos na molécula inicial, é preciso seguir a regra de Zaitsev para definir qual hidrogênio é removido. Essa regra diz que o hidrogênio eliminado será aquele do carbono menos hidrogenado.
Eliminação de água
É uma reação que acontece catalisada por ácido sulfúrico (um agente desidratante) e sob aquecimento. Nela ocorre a perda de uma molécula de água e a formação do alceno. Ela pode acontecer de forma intramolecular, ou seja, em uma única molécula (reação 4), ou intermolecular, entre duas moléculas de álcool (reação 5 da imagem), em que ocorre a formação de um éter.
Abaixo estão representadas as reações de eliminação mencionadas.
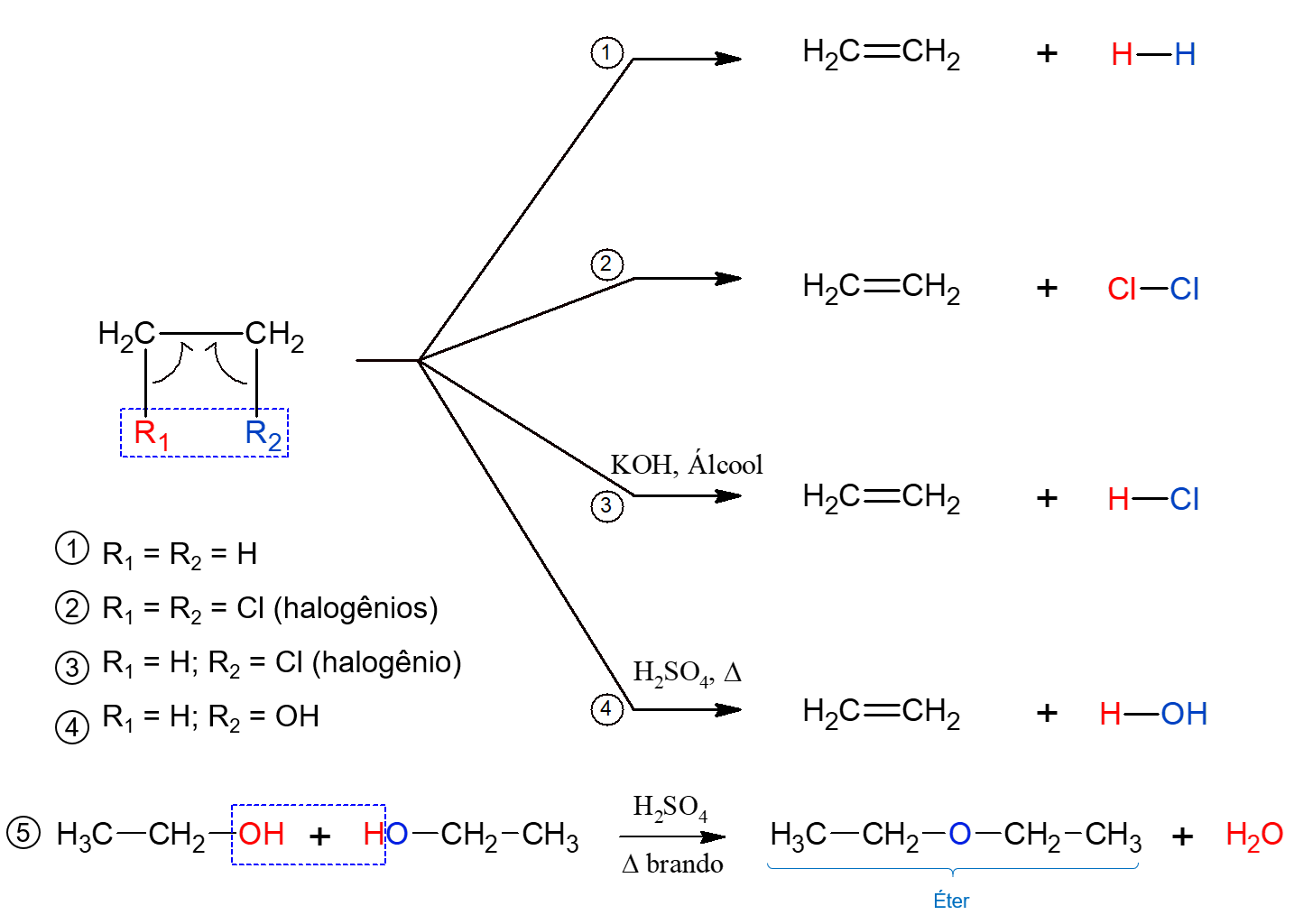
Reações orgânicas de oxidação
São reações onde ocorre o aumento do número de ligações entre carbono e oxigênio. Elas são catalisadas por um agente oxidante forte, geralmente o permanganato de potássio (KMnO4), dicromato de potássio (K2Cr2O7) ou o tetróxido de ósmio (OsO4). Esse agente é representado por [O] nas reações. As mais importantes são a oxidação de alcenos e de álcoois.
Oxidação branda de alcenos
Alcenos que reagem com o agente oxidante, em condições normais, tendem a liberar água e formar um di-álcool, resultante da quebra da ligação π da molécula. É uma reação de baixa energia.
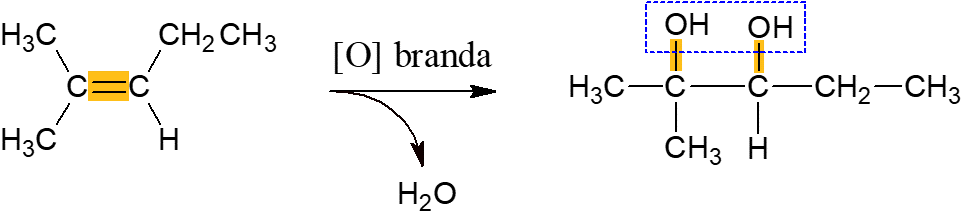
Oxidação energética de alcenos
De modo contrário, na oxidação energética, o agente oxidante é empregado em altas temperaturas e a reação é catalisada por ácidos fortes, resultando na quebra completa da molécula no local em que se encontra a ligação dupla do alceno, dando origem a duas moléculas diferentes. Os produtos formados dependem dos carbonos da molécula inicial. Carbonos terciários dão origem a cetonas, carbonos secundários formam ácidos carboxílicos, carbonos primários são oxidados a CO2 e água.
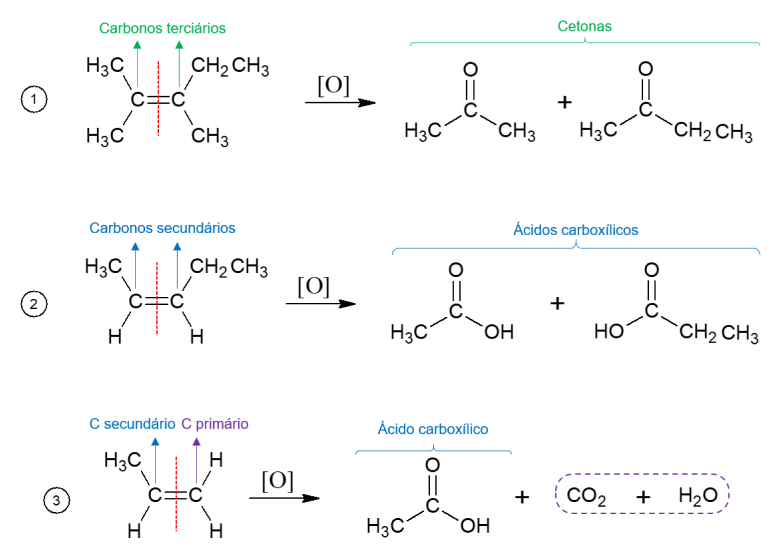
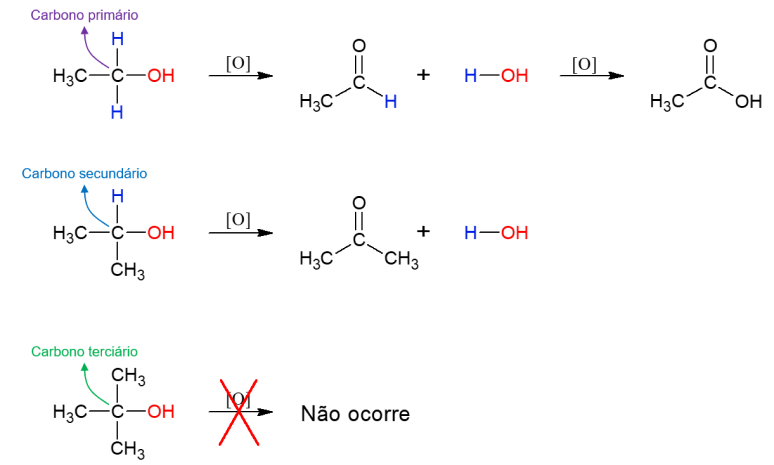
Oxidação de álcoois
Álcoois também podem sofrer reação com os agentes oxidantes, formando novos compostos. Se o álcool for primário, ocorre a formação de um aldeído. Porém, esse ainda pode ser oxidado em ácido carboxílico se permanecer no meio oxidante. Álcoois secundários dão origem a cetonas. Os álcoois terciários não reagem, já que não tem hidrogênio ligado ao carbono da hidroxila, o que permite a oxidação.
Essas são as principais reações orgânicas estudadas na disciplina. São muitos exemplos e a melhor maneira de entender todos é analisando diferentes exemplos com as mais variadas moléculas. Dessa forma é possível prever onde acontecerá cada etapa das reações.
Vídeos sobre as reações orgânicas estudadas
As reações orgânicas pode parecer um assunto denso e complicado. Para te ajudar, selecionamos alguns vídeos para assimilar melhor todos os conceitos. Acompanhe:
Como identificar o tipo de reação orgânica
Agora que você já tem conhecimento dos diferentes tipos de reações orgânicas, pode surgir a dúvida: como saber exatamente qual reação acontece olhando apenas para os reagentes e produtos? Nesse vídeo, essa dúvida é sanada. De modo prático você aprende a diferenciar as reações orgânicas.
Exercícios resolvidos sobre reações de eliminação
Um dos temas que mais caem em vestibulares e no ENEM está relacionado com as reações orgânicas. Nesse vídeo, temos exemplos de exercícios que envolvem as reações de eliminação, todos resolvidos e explicados para não restar dúvidas!
Qual o produto formado depois da oxidação de um álcool
Um álcool pode reagir com um agente oxidante para formar um aldeído, se for um álcool primário. Você consegue dizer qual o produto final formado após as reações propostas por esse exercício da FUVEST? Assista ao vídeo e confira a resolução.
Por fim, foi possível perceber a variedade de reações orgânicas que existe. A partir delas é possível obter diferentes compostos e isso possibilitou o avanço na indústria farmacêutica, por exemplo, já que a síntese de medicamentos foi uma alternativa encontrada para a dificuldade de extração dos bioativos de plantas. Estude também sobre as cadeias carbônicas e saiba como diferenciar uma cadeia saturada de uma insaturada.
Referências
Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente (2005) – Peter Atkins e Loretta Jones
Química: a ciência central (1999) – Theodore L. Brown, Eugene H. LeMay, Bruce E. Bursten e Julia R. Burdge
Química Orgânica (1976) – T. W. Graham Solomons
Química Orgânica – Volume 1 (1987) – Paula Yurkanis Bruice

Por Lucas Makoto Tanaka dos Santos
Bacharel em Química pela Universidade Estadual de Maringá (UEM), mestrando em Química Analítica, com ênfase em desenvolvimento de métodos analíticos, metabolômica e espectrometria de massas no Laboratório de Biomoléculas e Espectrometria de Massas (LaBioMass), na mesma universidade.
Tanaka dos Santos, Lucas Makoto. Reações Orgânicas. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/reacoes-organicas. Acesso em: 19 de May de 2026.
1. [UFV - 2002]
A reação de oxidação de um álcool de fórmula molecular C5H12O‚ com KMnO4 forneceu um composto de fórmula molecular C5H10O.
Assinale a opção que apresenta a correlação CORRETA entre o nome do álcool e o nome do produto formado.
a) 3-metilbutan-2-ol, 3-metilbutanal
b) pentan-3-ol, pentan-3-ona
c) pentan-1-ol, pentan-1-ona
d) pentan-2-ol, pentanal
e) 2-metilbutan-1-ol, 2-metilbutan-1-ona
Realizando as reações de oxidação dos álcoois propostos nas alternativas temos:
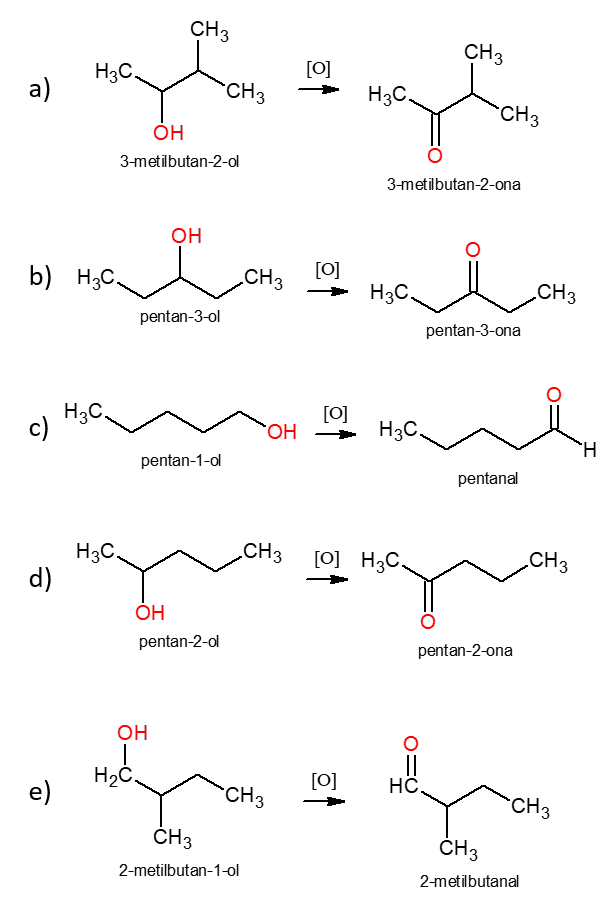
A única alternativa que o produto corresponde ao realmente formado é a letra b, pentan-3-ol, pentan-3-ona.
2. [UESPI]
A hidrogenação catalítica de uma ligação dupla é caracterizada como uma reação de:
a) eliminação.
b) adição.
c) transesterificação.
d) de saponificação.
e) substituição.
A hidrogenação corresponde a adição de hidrogênios a molécula, portanto, alternativa (B).