O benzeno é um hidrocarboneto aromático de fórmula molecular C6H6. Descoberto pela primeira vez por Michael Faraday em 1825, teve sua estrutura proposta somente em 1865 por Kekulé, determinando sua estrutura hexagonal. A seguir, vamos conhecer mais sobre esse composto muito importante para a química orgânica:
Publicidade
O que é o benzeno
O benzeno, em condições ambientes, é um líquido incolor e inflamável, de cheiro adocicado bastante característico e muito tóxico. É muito empregado na indústria como matéria-prima de polímeros, usado como aditivo de gasolina ou, ainda, na produção de tintas, detergentes, explosivos, entre outros.
Relacionadas
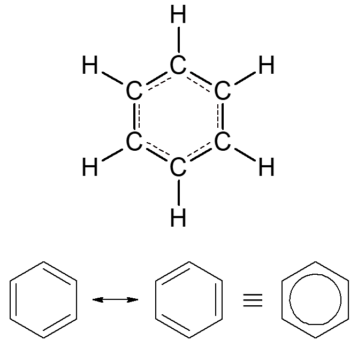
Sua fórmula estrutural é um hexágono de lados iguais, com um carbono em cada vértice, resultando na fórmula C6H6. Ela pode ser representada de diferentes formas, conforme a figura acima, por conta da ressonância que existe entre as ligações, ou seja, a alternância de posição da ligação ℼ.
Possui algumas propriedades interessantes, fazendo com que ele seja um dos principais compostos estudados na química orgânica.
- É um hidrocarboneto aromático e cíclico, além de ser insaturado, ou seja, possui ligações duplas;
- Sua temperatura de fusão é de 5,5 °C e a de ebulição é de 80,1 °C;
- Possui elevada volatilidade, ou seja, tende a passar para o estado gasoso com muita facilidade;
- Composto apolar e estável, por conta da ressonância entre as ligações duplas;
- Massa molar de 78,1 g/mol e densidade de 0,88 g/cm3 (menos denso que a água).
Tudo isso faz com que ele seja um dos principais compostos da química orgânica. É o principal percursor de diversas moléculas que possuem um anel aromático na estrutura, conforme reage com outros compostos em reações de adição ou substituição.
Nomenclatura de compostos com benzeno
A nomenclatura se dá de maneira simples, conforme a IUPAC (União Internacional de Química Pura e Aplicada). Primeiro, é preciso colocar o nome do grupo substituinte do anel aromático, em seguida completar com a palavra benzeno. Em casos em que há mais de um substituinte, a posição em que se encontram determina o prefixo do nome:
Publicidade
- Orto (o): quando os substituintes estão na posição 1 e 2.
- Meta (m): substituintes na posição 1 e 3.
- Para (p): substituintes na posição 1 e 4.
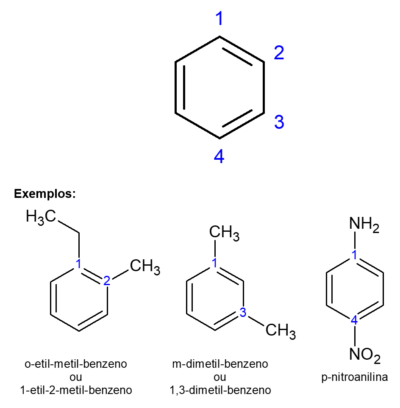
Observação: a p-nitroanilina recebe esse nome porque a amino-benzeno é popularmente chamada de anilina.
Onde encontramos o benzeno
Grande parte da concentração de benzeno presente na atmosfera é resultado da ação humana, pela emissão em indústrias ou como subproduto de queimadas. Ele também está presente na fumaça do cigarro. É um dos constituintes do petróleo, sendo encontrado na gasolina automotiva e em tintas.
A toxicidade do benzeno
É um composto carcinogênico, ou seja, se o período de exposição ao benzeno for longo, pode causar o aparecimento de câncer no organismo – principalmente na medula óssea, causando a leucemia. A curto prazo, o composto pode causar tonturas, arritmia cardíaca, desmaios ou sonolência e convulsões.
Publicidade
A exposição a essa substância se dá, na maioria das vezes, pela inalação, já que é um composto bastante volátil. Mas, se o líquido entrar em contato com a pele, pode causar dermatite e outros problemas relacionados à absorção da substância pelo organismo.
Benzeno é polar ou apolar?
Por conta de sua estrutura, assim como todos os hidrocarbonetos, o benzeno é apolar e, sendo assim, apresenta solubilidade muito baixa em água (que é polar), de apenas 0,8 g/L a 15 °C. Sua estrutura não apresenta heteroátomos capazes de realizar ligação de hidrogênio com a água, como O, F ou N. Por isso, o benzeno é usado como solvente orgânico de reações químicas, solubilizando outros compostos apolares.
Vídeos sobre o benzeno e suas propriedades
Agora que já estudamos o conteúdo, nada melhor que assistir a alguns vídeos que ajudem a assimilar o que foi estudado. Confira abaixo:
Os riscos do benzeno
O benzeno é uma substância presente em diferentes materiais do nosso cotidiano. Um exemplo disso é a gasolina, em que o benzeno pode ser adicionado para melhorar a octanagem do combustível. Saiba quais são os riscos envolvidos com a exposição desse composto químico perigoso.
Estrutura de ressonância do anel aromático
A estrutura molecular do benzeno sofre um fenômeno químico chamado de ressonância, em que as nuvens eletrônicas responsáveis pela formação da ligação do tipo ℼ deslocam-se entre os carbonos. Entenda melhor como esse efeito acontece e o porquê de as ligações químicas entre os átomos serem do mesmo tamanho, formando um hexágono perfeito.
Nomenclatura de compostos derivados do benzeno
Quando um anel aromático tem dois grupos substituintes em sua estrutura, a nomenclatura da molécula se dá de uma forma especial. Ela varia conforme as posições em que os substituintes estão. Saiba de uma vez por todas quando usar os nomes orto, meta e para na para nomear compostos derivados do benzeno.
Em síntese, o benzeno é um dos principais focos de estudo da química orgânica. Tanto por suas propriedades quanto pelas reações que pode sofrer, gerando outros compostos importantes. Estude também sobre as cadeias carbônicas e saiba tudo sobre estruturas saturadas ou insaturadas!
Referências
Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente (2005) – Peter Atkins e Loretta Jones
Química: a ciência central (1999) – Theodore L. Brown, Eugene H. LeMay, Bruce E. Bursten e Julia R. Burdge
Química Orgânica (1976) – T. W. Graham Solomons
Química Orgânica – Volume 1 (1987) – Paula Yurkanis Bruice

Por Lucas Makoto Tanaka dos Santos
Bacharel em Química pela Universidade Estadual de Maringá (UEM), mestrando em Química Analítica, com ênfase em desenvolvimento de métodos analíticos, metabolômica e espectrometria de massas no Laboratório de Biomoléculas e Espectrometria de Massas (LaBioMass), na mesma universidade.
Tanaka dos Santos, Lucas Makoto. Benzeno. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/benzeno. Acesso em: 09 de May de 2026.
1. [UNISINOS - RS]
Considere o seguinte composto:
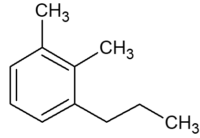
Sua nomenclatura correta é:
a) 1,2-etil-3-propilbenzeno
b) 1,2-dimetil-3-propilbenzeno
c) 1-propil-2,3-dimetilbenzeno
d) o-metil-m-propilbenzeno
e) m-dimetil-o-propilbenzeno
Alternativa correta: B
A estrutura é constituída de um benzeno com três substituintes, nas posições marcadas como 1, 2 e 3. São eles: 2 metil e 1 propil.
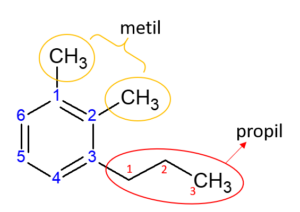
Os substituintes metil (-CH3) estão nas posições 1 e 2, já o propil (-CH2CH2CH3) está na posição 3 do benzeno. Sendo assim, a nomenclatura se dá em ordem alfabética, começando pelos dimetil. Ou seja, o nome fica 1,2-dimetil-3-propilbenzeno.
2. [FGV - SP]
A destilação de hulha produz uma série de compostos, um dos quais é um hidrocarboneto de massa molar (MM) 78 g.mol-1. Considerando-se que as massas molares do Carbono, do Hidrogênio e do Oxigênio são, respectivamente, 12, 1 e 16 g.mol-1, concluímos que esse hidrocarboneto é:
a) hex-1-eno.
b) benzeno.
c) pentano.
d) ciclopentano
e) hexano
Alternativa correta: B
Abaixo, estão representadas as estruturas das moléculas informadas, bem como suas fórmulas moleculares. A partir dessa informação, é possível calcular a massa molar (MM) de cada uma delas, tendo em mãos os valores das massas molares de cada um dos elementos que constituem a estrutura. O valor da MM está representado abaixo das fórmulas moleculares.
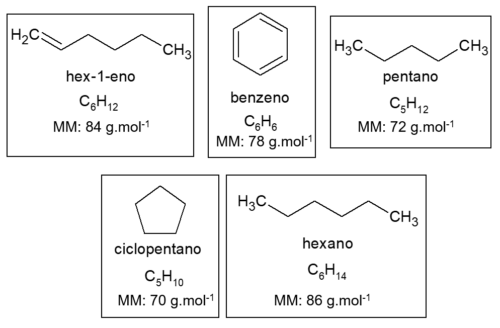
Entre todas as moléculas, o benzeno é o que apresenta a massa molar de 78 g.mol-1.