Em um sistema isolado do meio externo, isto é, quando não há troca de calor com o meio externo, ocorre a chamada transformação adiabática. Nesse processo, toda a energia interna é transformada em trabalho. Portanto, neste post, você aprenderá o que é transformação adiabática, sua fórmula, seu gráfico, exemplos e mais. Confira:
Publicidade
O que é transformação adiabática
A transformação adiabática é um processo termodinâmico no qual não há troca de calor entre um sistema e sua vizinhança. Ou seja, nesse tipo de transformação, o sistema termodinâmico não troca calor com o meio externo. No mesmo sistema, contudo, a pressão, o volume, a energia interna e a temperatura variam.
Relacionadas

As transformações adiabáticas estão presentes em diversas situações do nosso cotidiano. Por exemplo, ao espirrar um spray de aerossol, não há troca de calor com o meio externo, porém o volume, a pressão, a temperatura e a energia interna da lata variam.
Fórmula da transformação adiabática
A fórmula da transformação adiabática é obtida a partir da Primeira Lei da Termodinâmica. Assim:
![]()
Como Q = 0, então:
Publicidade
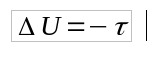
- Q: calor (J)
- ΔU: variação de energia interna (J)
- τ: trabalho (J)
A transformação adiabática também pode ser estudada em termos da variação da pressão e do volume, em que o produto entre os dois será uma constante.
Gráfico da transformação adiabática
O gráfico da transformação adiabática é obtido por meio do diagrama de Clapeyron ou diagrama P x V.
Publicidade
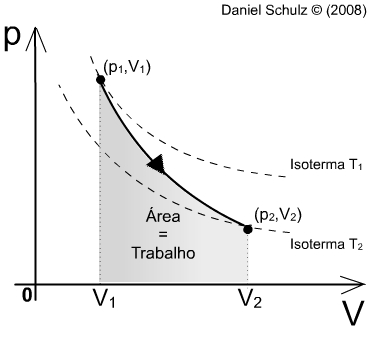
De maneira geral, o gráfico das adiabáticas mostra que uma transformação adiabática leva em consideração a variação da temperatura e do volume.
Exemplos de transformação adiabática
As transformações adiabáticas estão presentes em nosso cotidiano. Veja os exemplos a seguir:
Spray aerossol
Ao pressionar a válvula, o gás é expelido com uma velocidade muito alta. Isso faz diminuir a pressão do recipiente e, em consequência, a temperatura cai de maneira drástica.
Motor à combustão interna
Em motores à combustão interna, como o que está presente nos carros, os gases são comprimidos dentro do pistão. Dessa forma, a pressão sobre o gás aumenta e seu volume diminui. Durante esse processo, não há troca de calor com o ambiente.
Em um sistema real, não é possível que haja uma compressão ou uma expansão adiabática perfeita, porque o sistema sempre trocará um pouco de calor com o meio externo.
Vídeos sobre transformação adiabática
Chegou a hora de aprofundar seus conhecimentos sobre o tema desse texto. Para isso, assista aos vídeos que selecionamos:
Primeira Lei da Termodinâmica e as transformações
O professor Douglas relaciona a Primeira Lei da Termodinâmica e as transformações adiabáticas. Nesse vídeo, as trocas de energia são estudadas a partir dos mecanismos de troca de calor e de trabalho. Assim, é possível entender o que acontecerá com a energia interna do gás.
Experimento sobre a expansão adiabática
Para ilustrar o que acontece em uma expansão adiabática, o professor Claudio Furukawa realiza um experimento. Tal prática pode ser repetida e é ideal para feiras de ciências ou trabalhos de física experimental.
Equação de Clapeyron e as transformações adiabáticas
A equação de Clapeyron também é chamada de equação dos gases ideais. Sua fórmula relaciona a pressão, o volume, o número de mols, a temperatura e uma constante dos gases ideais. Por conta disso, é possível estudar as transformações gasosas a partir dessa fórmula. Nesse vídeo, o professor Marcelo Boaro explica como relacionar as transformações adiabáticas e a equação de Clapeyron.
Agora que você já aprendeu como acontecem as transformações adiabáticas, não se esqueça de ler também nosso post sobre a Primeira Lei da Termodinâmica!
Referências
Física II: termodinâmica e ondas (2016) – Hugh Young et al.
Transformação Adiabática – Daniel Schulz. Disponível em: https://www.if.ufrgs.br/~dschulz/web/adiabatica.htm. Acesso em: 13 jan. 2021

Por Hugo Shigueo Tanaka
Divulgador Científico e co-fundador do canal do YouTube Ciência em Si. Historiador da Ciência. Professor de Física e Matemática. Licenciado em Física pela Universidade Estadual de Maringá (UEM). Mestre em Ensino de Ciências e Matemática (PCM-UEM). Doutorando em Ensino de Ciências e Matemática (PCM-UEM).
Tanaka, Hugo Shigueo. Transformação adiabática. Todo Estudo. Disponível em: https://www.todoestudo.com.br/fisica/transformacao-adiabatica. Acesso em: 13 de May de 2026.
1. [Efomm]
Um gás ideal sofre uma expansão isotérmica, seguida de uma compressão adiabática. A variação total da energia interna do gás poderia ser nula se, dentre as opções abaixo, a transformação seguinte fosse uma
a) compressão isocórica;
b) expansão isocórica;
c) expansão isobárica;
d) compressão isobárica;
e) compressão isotérmica.
Resposta correta: D
Nesse caso, para que a variação da energia interna seja nula, a variação da temperatura também deve ser nula. Para isso, o gás deve sofrer uma compressão isobárica.
2. [Udesc]
Um gás ideal monoatômico, com n mols e inicialmente na tempertura absoluta T, sofre uma expansão adiabática até que sua temperatura fique a um terço da sua temperatura inicial.
Logo, o gás:
a) Absorveu uma quantidade de calor igual a nRT.
b) Se expandiu isobaricamente.
c) Realizou trabalho liberando uma quantidade de calor igual a nRT.
d) Se expandiu aumentando sua energia interna de nRT.
e) Realizou trabalho e a sua energia interna diminuiu de nRT.
Resposta correta: E
Como o gás sofreu uma expansão, ou seja, aumentou o volume, então ele realizou trabalho, mas o processo foi adiabático. Ou seja, não houve troca de calor com o meio externo. Dessa forma, o trabalho realizado pelo gás foi às custas de sua energia interna.