Calor específico é a quantidade de energia térmica necessária para que uma grama de certa substância varie a sua temperatura em um grau.
Publicidade
O que é o calor específico
O calor específico de uma substância pode ser definido a partir de sua capacidade térmica. Por definição, o calor específico é a razão entre a capacidade térmica e a massa da substância.
Relacionadas
A capacidade térmica, por sua vez, é a grandeza física que relaciona a energia térmica recebida pela substância e a sua variação de temperatura.
O calor específico pode ser aplicado em diversas áreas do conhecimento, desde a engenharia até a gastronomia. Dominar os conceitos de calor específico significa, por exemplo, escolher de maneira mais proveitosa determinado material para o isolamento térmico.
Quanto maior é o calor específico de uma substância maior será a quantidade de energia necessária para que sua temperatura varie. Por exemplo, em um dia ensolarado na praia, percebemos que a areia está em uma temperatura superior à da água. Isso acontece porque o calor específico da água é muito maior que o da areia. Ou seja, para que a temperatura da água varie, é necessário fornecer muito mais energia.
Portanto, uma substância ter um calor específico mais alto significa que ela precisará de mais energia para que ocorra variação de sua temperatura. De maneira parecida, uma substância com calor específico baixo necessitará de menos energia para variar a sua temperatura.
Publicidade
Fórmula
A diferença entre um calor específico baixo e um calor específico alto pode ser observada matematicamente. Assim, vejamos a fórmula do calor específico:
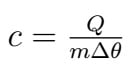
Onde:
Publicidade
- c: calor específico (cal/g°C ou J/kg K)
- Q: quantidade de calor (cal ou J)
- m: massa da substância (g ou kg)
- Δθ: variação da temperatura (°C ou K)
Note que existem duas unidades de medida para cada grandeza física da fórmula do calor específico. Elas estão nas unidades de medida usuais (cal, g e °C) e nas unidades de medida do Sistema Internacional (J, kg e K).
Capacidade térmica e calor específico
O calor específico é uma grandeza física que não varia conforme as dimensões da substância. Ou seja, ele é uma grandeza intensiva. Assim, 1 g de água ou 1000 kg de água terão o mesmo calor específico.
Já a capacidade térmica é uma grandeza física que depende da massa dessa substância. Consequentemente, ela depende das dimensões do corpo. Ou seja, a capacidade térmica é uma grandeza extensiva. Assim, 1 g de água terá menos capacidade térmica que 1000 kg da mesma substância.
Porém, o calor específico pode ser definido a partir da capacidade térmica. Por sua vez, corresponde à razão entre a capacidade térmica e a massa da substância. Matematicamente:
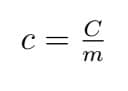
Onde:
- c: calor específico (cal/g°C ou J/kg K)
- C: capacidade térmica (cal/°C ou J/K)
- m: massa da substância (g ou kg)
Tabela de calor específico
O calor específico de uma determinada substância é uma característica intrínseca da sua composição molecular. Ele depende, portanto, dos graus de liberdade das moléculas, da massa molar, das ligações de hidrogênio, das impurezas da substância etc.
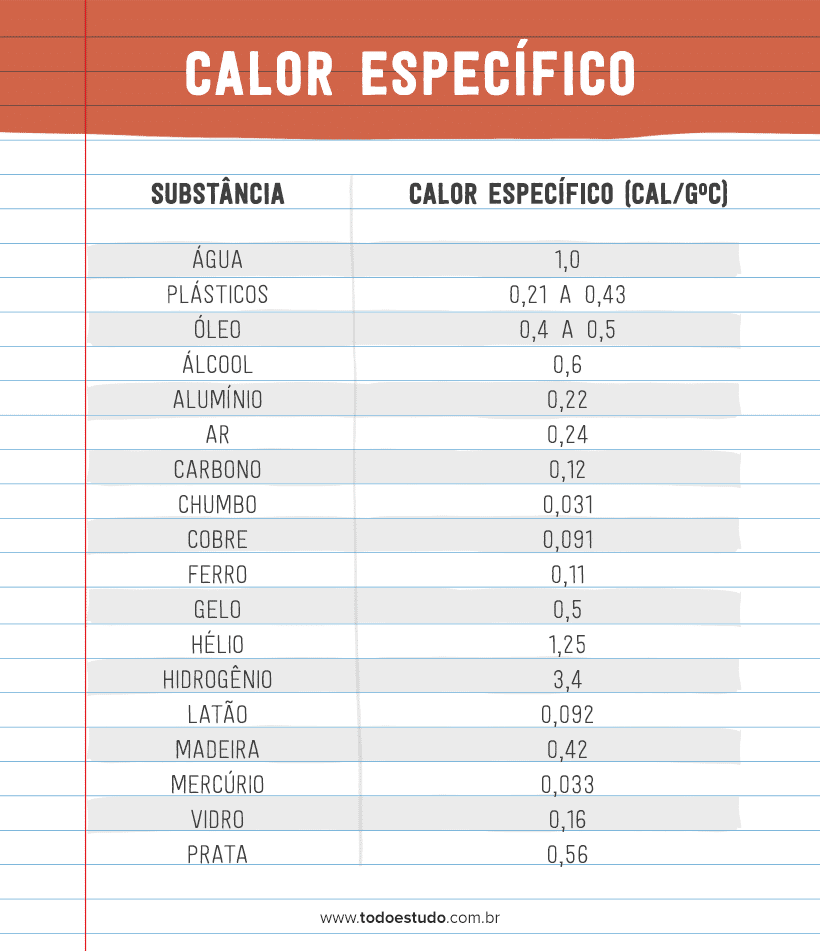
Note as diferenças entre o calor específico das substâncias. Além disso, é importante notar que o calor específico não é a quantidade de energia necessária para aumentar a temperatura da substância. É a quantidade de temperatura necessária para variar a temperatura do corpo.
Vídeos sobre calor específico
Agora que já aprendemos os conceitos básicos sobre calor específico. Vamos aprofundar nossos conhecimentos deste conteúdo com os vídeos sugeridos:
Experimentos sobre calor específico e capacidade térmica
Veja algumas experiências simples sobre calor específico e capacidade térmica.
Aprofundamento teórico em Calor Específico
Aprofunde seus conhecimentos sobre calor específico.
Quantidade de calor e calor específico
Saiba como aplicar os conceitos de calor específico em outros conteúdos de física, como a quantidade de calor.
O calor específico está muito presente em nosso cotidiano e, além disso, é um conceito fundamental para a compreensão da termodinâmica. Para continuar seus estudos, veja nossa matéria sobre a Primeira Lei da Termodinâmica.
Referências
YOUNG, Hugh D. et al. Física II: Termodinâmica e Ondas. São Paulo: Addison Wesley. 2016
LUZ, Gelson. Calor específico. Disponível em: https://www.materiais.gelsonluz.com/2018/09/calor-especifico.html.

Por Hugo Shigueo Tanaka
Divulgador Científico e co-fundador do canal do YouTube Ciência em Si. Historiador da Ciência. Professor de Física e Matemática. Licenciado em Física pela Universidade Estadual de Maringá (UEM). Mestre em Ensino de Ciências e Matemática (PCM-UEM). Doutorando em Ensino de Ciências e Matemática (PCM-UEM).
Tanaka, Hugo Shigueo. Calor específico. Todo Estudo. Disponível em: https://www.todoestudo.com.br/fisica/calor-especifico. Acesso em: 11 de May de 2026.
1. [Eear]
Duas porções de líquidos A e B, de substâncias diferentes,, mas de mesma massa, apresentam valores de calor específico iguais a 0,58 cal/g°C e 1,0 cal/g°C. Se ambas receberem a mesma quantidade de calor, sem contudo sofrerem mudanças de estado físico, podemos afirmar corretamente que:
a) a porção do líquido A sofrerá maior variação de temperatura do que a porção do líquido B.
b) a porção do líquido B sofrerá maior variação de temperatura do que a porção do líquido A.
c) as duas porções, dos líquidos A e B, sofrerão a mesma variação de temperatura.
d) as duas porções, dos líquidos A e B, não sofrerão a nenhuma variação de temperatura.
Da definição do calor específico podemos concluir que o líquido com menor terá uma variação de temperatura maior. Assim, o líquido A sofrerá uma variação de temperatura maior que o líquido B.
Alternativa correta: A
2. [UEPG]
Quanto à transferência de energia térmica, assinale o que for correto.
01) Corpos diferentes apresentarão temperaturas diferentes após recebimento de calor num determinado tempo
02) A energia cinética média das partículas individuais está diretamente relacionada com a temperatura de uma substância.
04) Quanto maior o calor específico de uma substância, maior será a dificuldade de fazer variar sua temperatura.
08) O calor específico é de maior valor nas substâncias sólidas do que nas substâncias líquidas.
01) Incorreta. A variação de temperatura depende da quantidade de calor recebida e da capacidade térmica do corpo. Se dois corpos diferentes apresentarem a mesma razção entre quantidade de calor e capacidade térmica (Q/C), terão a mesma variação de temperatura.
02)Correta
04)Correta
08) Incorreta. Basta pensar no calor específico da água em estado líquido (1,0 cal/g°C) e no calor específico do alumínio em estado sólido (0,22 cal/g°C).