Muitos cientistas buscaram entender algumas situações que envolviam a temperatura, volume e pressão de um determinado sistema. Com isso foi possível o desenvolvimento da termodinâmica, conteúdo esse que estudaremos aqui. Assim, vamos abordar o que ela é, suas leis e alguns alguns sistemas termodinâmicos.
Publicidade
O que é termodinâmica
A termodinâmica é o ramo da física que estuda as transformações de energia em sistemas macroscópicos. Porém, seu objetivo inicial dela era a de estabelecer relações entre calor e trabalho.
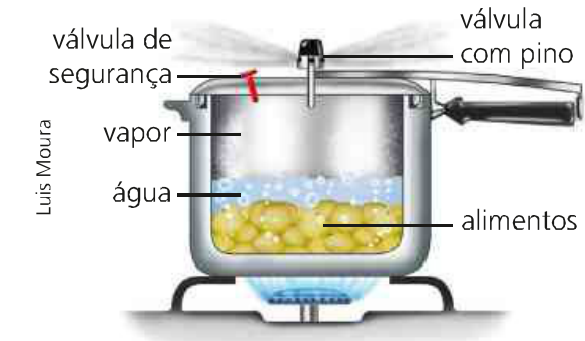
Temos como exemplo uma panela de pressão cozinhando algum alimento. Nesse processo, é mantido o volume constante e com o fornecimento de energia em forma de calor através do fogo se varia a temperatura e a pressão do sistema. Com isso, a energia transferida aquece a água fazendo com que o alimento seja preparado.
Sistemas Termodinâmicos
Antes de mais nada, precisamos entender um conceito conhecido como sistema termodinâmico para podermos entender a termodinâmica.
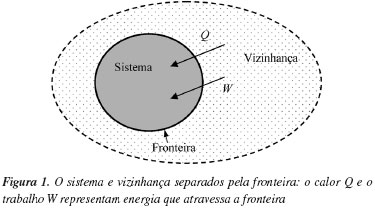
Um sistema termodinâmico é toda a região do espaço que se deseja estudar e que é separado por uma superfície chamada de fronteira, que separa o sistema do resto do universo. Podemos indicar tal sistema conforme sua relação de troca de energia com a vizinhança. Logo:
Publicidade
- Isolado: não troca energia nem matéria com o meio externo;
- Fechado: sistema que troca energia, mas não matéria com o meio externo;
- Aberto: é aquele que troca energia e/ou matéria com o meio externo;
- Termicamente isolado: esse tipo não troca calor com a vizinhança, ainda que nele possa ocorrer alguma modificação.
Lei Zero da Termodinâmica
Imagine a seguinte situação, conforme a figura a seguir, com dois corpos de mesmo material, mesma massa mas com temperaturas diferentes. O que aconteceria se esses corpos forem colocados em contato?
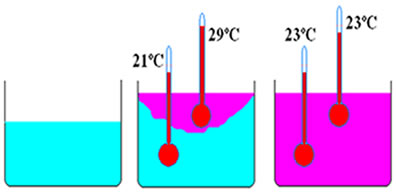
Pela lei zero da termodinâmica, esses corpo entram em equilíbrio térmico, ou seja, atingem a mesma temperatura depois de um certo tempo. Em outras palavras, essa lei descreve como acontecem as trocas de calor entre os corpos.
Publicidade
Primeira Lei da Termodinâmica
Se um sistema gasoso recebe calor do meio externo, essa energia pode ser armazenada para que exista a possibilidade de realização de trabalho.
![]()
Na expressão da primeira lei acima, temos que ∆U é a variação da energia interna do sistema, Q é a quantidade de calor recebida ou cedida e τ é o trabalho realizado ou sofrido pelo sistema.
Segunda Lei da Termodinâmica
De um modo geral, nós estamos envoltos de coisas que utilizam a segunda lei da termodinâmica a nosso favor. Um exemplo disso são os motores a combustão de carros, caminhões, motos e muitas outras máquinas. Além disso, refrigeradores, como geladeiras, utilizam esse princípio. Dessa forma, essa lei está relacionada a esses motores que realizam um certo ciclo para realizar trabalho.
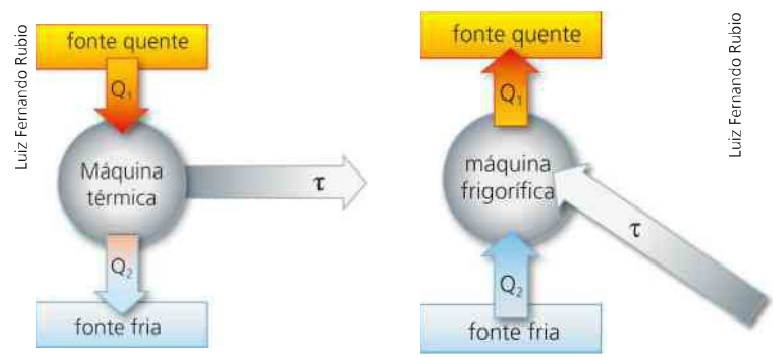
No início dos estudos sobre a termodinâmica, descobriu-se que nem todo o calor era transformado em trabalho. Essa energia que se perdia do sistema para o meio externo foi chamada de entropia, que é a razão entre a quantidade de calor trocada com o sistema e a temperatura absoluta inicial do sistema.
Com esses estudos foi possível enunciar a segunda lei da seguinte forma:
O calor flui espontaneamente da fonte quente para a fonte fria; para ocorrer o contrário, é necessário realizar trabalho externo.
Conforme a figura acima, podemos entender como as máquinas térmicas funcionam. No primeiro caso (máquina térmica) o calor flui da fonte quente para a fonte fria, realizando assim trabalho. No segundo caso (máquina frigorífica) ocorre o processo inverso, ou seja, o calor vai da fonte fria para a fonte quente, mas para que isso aconteça é necessário a realização de um trabalho externo, como um motor.
Terceira Lei da Termodinâmica
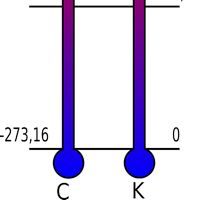
Um corpo pode chegar a um estado de total “pausa” em seu movimento. Esse fenômeno ocorre quando o corpo chega a temperatura de zero absoluta, ou seja, em 0 Kelvin. Em outras palavras:
Existe uma escala absoluta de temperatura que tem um mínimo definido como zero absoluto, no qual a entropia de todas as substâncias é a mesma.
Videoaulas sobre termodinâmica
Para um maior entendimento da termodinâmica, podemos utilizar os vídeos abaixo sobre tal assunto.
Primeira lei da termodinâmica
Aqui, são apresentados os conceitos e explicações sobre a primeira lei da termodinâmica.
Máquinas térmicas
Neste vídeo podemos entender um pouco melhor sobre o conceito de máquinas térmicas.
Segunda lei da termodinâmica
Por fim, esse vídeo apresenta todo o conceito da segunda lei da termodinâmica.
Muitas coisas das nossas vidas foram facilitadas pela termodinâmica. Sem ela, não existiriam os motores como vemos hoje, as geladeiras, entre muitas outras coisas. Portanto, podemos concluir que esse assunto não é apenas importante para os vestibulares mas também para o nosso entendimento do mundo.
Referências
As faces da física – Wilson Carron e Osvaldo Guimarães;
Física para o ensino médio, volume 2 – Kazuhito Yamamoto e Luiz Felipe Fuke.

Por Guilherme Santana da Silva
Graduado no curso de Física pela Universidade Estadual de Maringá. Professor assistente em um colégio de ensino médio e preparatório para os vestibulares. Nas horas vagas se dedica à vida religiosa, praticar mountain bike, tocar bateria, dar atenção à família e cuidar de suas duas gatinhas Penélope e Mel.
Santana, Guilherme. Termodinâmica. Todo Estudo. Disponível em: https://www.todoestudo.com.br/fisica/termodinamica. Acesso em: 11 de May de 2026.
1. [ITA-SP]
Considere uma mistura de gases H2 e N2 , em equilíbrio térmico. Sobre a energia cinética média e sobre a velocidade média das moléculas de cada gás, pode-se concluir que:
a) as moléculas de H2 e N2 tem a mesma energia cinética média e a mesma velocidade média.
b) Ambas tem a mesma velocidade média, mas as moléculas de N2 tem maior energia cinética média.
c) Ambas tem a mesma velocidade média, mas as moléculas de H2 tem maior energia cinética média.
d) Ambas tem a mesma energia cinética média, mas as moléculas de N2 tem maior velocidade média.
e) Ambas tem a mesma energia cinética média, mas as moléculas de H2 tem maior velocidade média.
O equilíbrio térmico ocorre quando TH = TN. Como a energia cinética depende da temperatura, ambas possuem a mesma energia cinética.
A energia cinética de uma molécula de gás é dada por
v² = (3RT)/M
Como a massa de H2 é menor do que a massa de N2, a velocidade das moléculas de H2 é maior.
RESPOSTA: e)
2. [UF - RN]
Dentro de uma sala com ar condicionado, a temperatura média é de 17 ºC. No corredor ao lado da sala, a temperatura média é 27 ºC. Tanto a sala quanto o corredor estão a mesma pressão.
Sabe-se que num gás, a energia cinética média das partículas que o compõem é proporcional à temperatura e que sua pressão é proporcional ao produto da temperatura pelo número de partículas por unidade de volume.
Com base nesses dados, pode-se afirmar que:
a) a energia cinética média das partículas que compõem o ar é maior no corredor, e o número de partículas por unidade de volume é menor na sala.
b) A energia cinética média das partículas que compõem o ar é maior no corredor, e o número de partículas por unidade de volume é maior na sala.
c) A energia cinética média das partículas que compõem o ar é maior na sala, e o número de partículas por unidade de volume é maior no corredor.
d) A energia cinética média das partículas que compõem o ar é maior na sala, e o número de partículas por unidade de volume é menor no corredor.
A energia cinética média das partículas no corredor é maior que na sala pois tem uma maior temperatura. Temos que
p = KTN
Onde N é o número de partículas por unidade de volume e T a temperatura do ambiente. Dessa forma
pc = ps
KcTcNc = KcTcNc
Mas como Tc > Ts então Ns > Nc
RESPOSTA: b)