O soluto e solvente fazem parte de uma solução química. Estes dois componentes será a parte mais importante da mistura homogênea.
Publicidade
Essas misturas químicas são soluções (ou dispersões) homogêneas, e terão sua formação dependente do soluto e solvente. Basicamente, o soluto será a substância a ser dissolvida, enquanto o solvente será a responsável por dissolvê-la.
Coeficiente de Solubilidade
Antes de compreender com a certeza o soluto e solvente, é preciso entender sobre o coeficiente de solubilidade. Esse coeficiente estará diretamente ligado ao limite de um soluto a ser adicionado à mistura.
É chamado de coeficiente de solubilidade toda a quantidade necessária de soluto que sature (ou venha a saturar) a quantidade ideal de solvente determinada pela temperatura.
O coeficiente de solubilidade será inteiramente dependente da temperatura, e variará de acordo com ela. Pode-se, assim, aumentar ou diminuir, de acordo com alterações na temperatura e do dado soluto.
Entendendo soluto e solvente
A diferença entre soluto e solvente é bem simples e prática. Enquanto o solvente será a substância a realizar a dissolução, o soluto será a substância a ser dissolvida.
Essa dissolução (e consequente mistura) de soluto em solvente ocorrerá a partir da interação entre moléculas. O exemplo de solvente mais conhecido é a água, esta apelidada de “solvente universal”.
Publicidade
O apelido se deve ao fato de ela ter a capacidade de dissolução de uma gama de substâncias diferentes.
Soluto
O soluto é a substância dispersora, aquela a ser dissolvida. Assim, ela distribui-se no interior de outra substância, sob forma de pequenas partículas.
Tais partículas do soluto apresentarão o diâmetro de até 1 nanômetro (1nm = 10-9 metros). Dessa forma, mesmo com o microscópio mais potente atualmente seria possível assistir mesmo que a maior fase das soluções.
Publicidade
Técnicas físicas não são capazes de separar as misturas entre soluto e solvente. Ou seja, filtração, centrifugação e decantação não são capazes de separar a mistura. Apenas a técnica química da destilação é capaz de separar a solução.
Solvente
O solvente, por outro lado, é apenas a substância dispersante da solução. Ela permitirá a distribuição das moléculas em seu interior.
Exemplos de soluto e solvente
Existem três misturas pontuais para exemplificar soluto e solvente. São elas, assim:
Vinagre
- Solvente: Água
- Soluto: Ácido Acético
Soro Fisiológico
- Solvente: Água
- Soluto: Cloreto de Sódio
Água e Açúcar
- Solvente: Água
- Soluto: Açúcar
Classificação das soluções
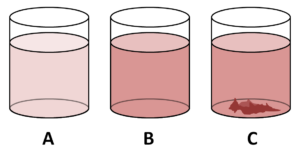
- Solução saturada: soluções que acabaram atingindo limite do coeficiente de solubilidade, podendo apresentar precipitado.
- Solução Supersaturada: mais soluto dissolvido do que a saturada, apresentando nítido precipitado.
- Solução insaturada: soluto não atingiu o coeficiente de solubilidade, podendo ser acrescentado mais soluto para atingir equilíbrio.
Referências
SALVADOR, Edgard e USBERCO, João. Química, volume único. 1ª edição, Editora Saraiva, São Paulo-SP, 2006. 672 p.

Por Mateus Bunde
Graduado em Jornalismo pela Universidade Federal de Pelotas (UFPel), Especialista em Linguagens pelo Instituto Federal Sul-Rio-Grandense (IFSul) e Mestrando em Comunicação pela Universidade do Porto, de Portugal (UP/PT).
Bunde, Mateus. Soluto e Solvente. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/soluto-e-solvente. Acesso em: 03 de May de 2026.
01. [ITA] Considere cada um dos procedimentos realizados em temperatura ambiente e sob vigorosa agitação:
I. 1 g de açúcar sólido misturado com 1 L de água.
II. 1 g de cloreto de sódio sólido misturado com 1 L de água.
III. 0,5 L de solução aquosa de açúcar misturado com 0,5 L de água.
IV. 0,2 L de etanol anidro misturado com 0,8 L de gasolina.
V. Injeção de HCl gasoso em 1 L de água.
VI. Injeção de O2 gasoso em 1 L de água.
Assinale a opção que associa CORRETAMENTE os procedimentos acima com os fenômenos listados abaixo:
a. dissolução sem dissociação iônica;
b. somente dispersão grosseira;
c. diluição;
d. dissolução com dissociação iônica.
a) Ia; IId; IIIc; IVa: Vd; VIa
b) c; IIc; IIIc; IVa: Vc; VIc
c) Ic; IIa; IIId; IVb; Va; VId
d) Ia; IIa; IIIa; IVb; Va; VIa
e) Id; IId; IIIa; IVc; Vd; VId
02. [UFPE] Uma solução composta por duas colheres de sopa de açúcar (34,2 g) e uma colher de sopa de água (18,0 g) foi preparada. Sabendo que:
Massa molar da sacarose = 342,0 g mol-1,
Massa molar da água = 18,0 g mol-1,
Ponto de fusão da sacarose = 184 °C e Ponto de fusão da água = 0 °C,
podemos dizer que:
1) A água é o solvente, e o açúcar, o soluto.
2) O açúcar é o solvente, uma vez que sua massa é maior que a da água.
3) Em temperatura ambiente, o açúcar não pode ser considerado solvente por ser um composto sólido.
Está(ão) correta(s):
a) 1 apenas
b) 2 apenas
c) 3 apenas
d) 1 e 3 apenas
e) 1, 2 e 3
01. [A]
02. [D]