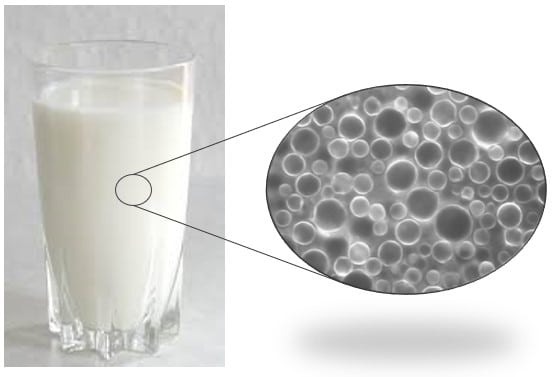
Ao olharmos para um copo de leite, enxergamos uma solução homogênea, mas se analisarmos uma gota em um microscópio, percebemos que, na verdade, se trata de uma mistura heterogênea de gotículas de gordura dispersas em uma solução aquosa, numa mistura conhecida como coloide do tipo emulsão. Vamos entender mais sobre os sistemas coloidais a seguir.
Publicidade
O que são coloides?
Os coloides (ou ainda dispersão coloidal) são os sistemas onde um ou mais componentes possuem tamanho entre 1 a 1000 nanômetros (nm), isto é, entre 1×10-9 m e 1×10-6m. Tais partículas podem ser desde íons até moléculas.
Relacionadas
Essa mistura foi estudada pela primeira vez pelo químico escocês Thomas Graham, em 1861, que percebeu uma característica incomum de substâncias – como amido, cola, gelatina e albumina do ovo – ao se difundirem vagarosamente em água, diferente de outras como o açúcar. Por conta disso, então, propôs o nome coloide, que vem do grego “kollas” (cola).
Os coloides, por conta de seu tamanho, não podem separados de uma solução por filtração comum, visto que passam pelos poros dos filtros. Nesse sentido, também não sofrem o processo de decantação, ou seja, não se sedimentam no fundo de um recipiente. Isso faz com que os sistemas coloidais tenham aparência de um líquido homogêneo.
Classificação dos coloides
Antes de mais nada, para explorarmos a classificação dos diferentes tipos de coloides, precisamos entender que são compostos de duas fases: a fase dispersa e o dispersante. A fase dispersa diz respeito ao componente das partículas coloidais. Já o dispersante é a fase contínua, ou seja, o meio em que a fase dispersa se encontra. Ambos podem ser compostos que estão no estado sólido, líquido ou gasoso.
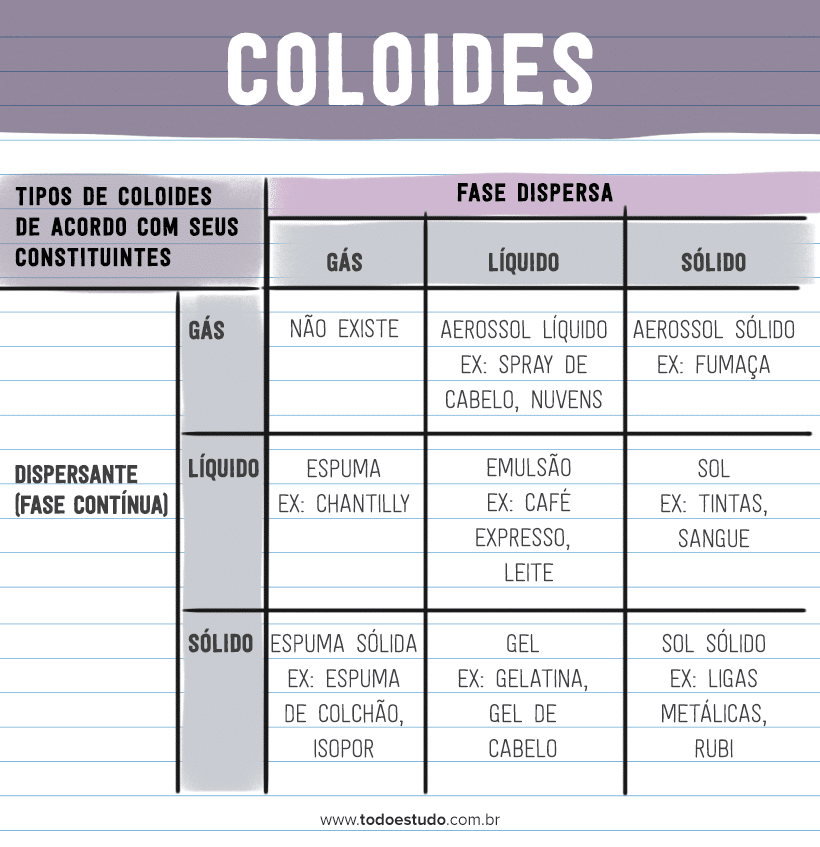
- Aerossol líquido: são constituídos de um líquido disperso em um meio gasoso. As nuvens, produtos em spray em geral e nevoeiros são exemplos desse tipo de sistema coloidal no qual, geralmente, a água está em suspensão no ar (ou em outro gás);
- Aerossol sólido: ocorre quando partículas sólidas estão em suspensão num gás. É o caso da fumaça, onde a fuligem é dispersa no ar;
- Espuma: diz respeito a um gás disperso em um líquido, como no caso de chantilly e espuma de barbear que incorporam o gás existente dentro da lata com o líquido, seja este o creme de leite ou o creme de barbear;
- Emulsão: é quando um líquido está disperso em outro. Ambos líquidos precisam ser imiscíveis para formar essa mistura coloidal. São exemplos o leite e a maionese;
- Sol: quando um sólido está em suspensão em um líquido, chamamos de sol. É o caso de muitas tintas, onde o pigmento em pó é incorporado em um tipo de resina base, formando um líquido viscoso e colorido que utilizamos na pintura de quadros e paredes;
- Espuma sólida: pode parecer estranho, mas é o caso do isopor. Partículas gasosas estão dispersas em um componente sólido. No caso do isopor, a fase sólida é composta de um polímero chamado de poliestireno (PS). Além deste, a pedra-pome é outro exemplo de espuma sólida;
- Gel: corresponde a líquidos suspensos em sólidos. É o caso da própria gelatina, em que a água é incorporada entre as moléculas do polímero que a constitui, o colágeno;
- Sol sólido: é quando um sólido está disperso em outro. Como exemplo, podemos citar alguns cristais – como rubi que possui óxido de cromo – e outros metais dispersos em sua composição.
Existe uma infinidade de coloides, mas aqui estão listados apenas alguns exemplos. Então, veremos agora algumas características que nos ajudam a entender melhor sobre esse tipo de mistura.
Publicidade
Características dos coloides
Existem alguns aspectos típicos dos coloides que contribuem para a natureza global de um sistema coloidal, isto é, são necessárias para que um sistema seja chamado de coloide.
Estabilidade
Os coloides são relativamente estáveis na natureza. As partículas da fase dispersa estão em um estado de movimentação contínuo, chamado de movimento Browniano, portanto continua suspenso em solução.
Capacidade de filtragem
Por conta de seu tamanho, os coloides não são filtrados por filtros comuns, passam com facilidade pelos poros do papel. Sendo assim, é necessário a utilização de filtros especiais, conhecidos como ultrafiltros.
Publicidade
Natureza heterogênea
Como são constituídos de duas fases, os coloides, em nível microscópico, possuem caráter heterogêneo, sendo possível distinguir entre as duas fases componentes.
Aparência homogênea
Mesmo que tenha partículas suspensas em solução, a aparência dos coloides corresponde a uma solução homogênea. As partículas são tão pequenas que não são visíveis a olho nu.
Efeito Tyndall
Essa característica óptica dos sistemas coloidais diz respeito ao espalhamento de luz provocado pelas partículas dispersas nos coloides e, por conta desse espalhamento, é possível ver o feixe de luz que incide sobre o sistema. Em soluções verdadeiras, como a água pura por exemplo, esse efeito não ocorre, já que não existe partículas em suspensão.

Dessa forma, sabemos agora de algumas características que diferenciam os coloides de soluções verdadeiras. Veremos agora algumas de suas aplicações.
Usos e aplicações dos coloides
Os coloides estão muito presentes no cotidiano, em vários produtos de limpeza, alimentícios e até mesmo no tratamento de água. Alguns exemplos:
- Indústria alimentícia: diversos alimentos são compostos de sistemas coloidais. Leite, manteiga, gelatinas, café, chantilly são alguns exemplos, mas a gama é bastante diversa;
- Produtos de higiene: as espumas de barbear, gel de cabelo, desodorantes aerossóis, shampoos, entre outros, são exemplos de sistemas coloidais aplicados na higiene e cuidados pessoais. É a maneira prática de combinar muitos componentes em um único produto ou deixar tal item mais fácil de aplicar;
- Tratamento de água: nesse caso, os coloides são os interferentes do processo de tratamento da água potável e precisam ser retirados. Mesmo depois de etapas de decantação e filtração, a água ainda apresenta uma opacidade causada por partículas em suspensão que não foram filtradas, os coloides. Para removê-los, um agente coagulante é adicionado, que desestabiliza as partículas, fazendo com que elas se aglomerem e se sedimentem no fundo dos tanques.
- Produção de polímeros: na indústria química, muitas vezes os coloides são empregados para produção de polímeros, como isopor (poliestireno expandido).
- No organismo: o sangue é um tipo de coloide (sol), onde os diferentes constituintes como hemácias, glóbulos brancos e plaquetas estão suspensos numa solução aquosa (o plasma).
- Tintas em geral: as tintas são nada mais que soluções coloidais, onde o pigmento (pó, no estado sólido), é disperso em um meio líquido.

Assim como já comentado, as aplicações dos coloides são infinitas. Um fato fascinante que nos mostra que a química está presente em tudo no nosso dia-a-dia.
Vídeos sobre as dispersões coloidais
Vamos conferir agora alguns vídeos sobre a matéria para entendermos melhor sobre os conceitos envolvidos.
O que são os coloides?
Neste vídeo, temos um apanhado geral do assunto, explicando esse tipo de mistura.
Propriedades e os diferentes tipos de coloides
Aqui são explicados os diferentes tipos de coloides, bem como suas propriedades
Como dispersões coloidais são sistemas heterogêneos?
Neste vídeo, temos uma explicação com relação aos diferentes tipos de dispersões e, nesse sentido, o motivo pelo qual os sistemas coloidais são misturas heterogêneas.
Em conclusão, conhecemos melhor sobre esse tipo de mistura que à primeira vista parece ser homogênea. Entretanto, quando analisamos mais a fundo, percebemos que se trata de uma mistura em que há a separação de fases das partículas envolvidas, mas estas são tão pequenas que não as enxergamos. Não pare de estudar por aqui! Veja mais sobre um dos tipos de sistemas coloidais e estude sobre emulsão.
Referências
Colloids and Colloidal Systems in Human Health and Nutrition – Robert O. Young
Físico-Química – Ira N. Levine
Princípios de química: questionando a vida moderna e o meio ambiente – Atkins, P. W., Jones, L.
Química volume único – João Usberco e Edgard Salvador
The Tyndall Effect – Niranjani Devarajan

Por Lucas Makoto Tanaka dos Santos
Bacharel em Química pela Universidade Estadual de Maringá (UEM), mestrando em Química Analítica, com ênfase em desenvolvimento de métodos analíticos, metabolômica e espectrometria de massas no Laboratório de Biomoléculas e Espectrometria de Massas (LaBioMass), na mesma universidade.
Tanaka dos Santos, Lucas Makoto. Coloides. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/coloides. Acesso em: 01 de May de 2026.
1.
Classifique os coloides a seguir em aerossol, emulsão, espuma, sol ou gel, considerando a fase dispersa e o dispersante.
I – Chantilly
II – Gel de cabelo
III – Leite
IV – Sangue
V – Placa de bronze
VI – Cristal de rubi
VII – Nevoeiro
I – Espuma (gás disperso em um líquido)
II – Gel (líquido disperso em um sólido)
III – Emulsão (liquido disperso em outro líquido)
IV – Sol (sólido disperso em um líquido)
V – Sol sólido, uma vez que o bronze é uma liga metálica de cobre e estanho (sólido disperso em outro sólido)
VI – Sol sólido)
VII – Aerossol líquido (líquido disperso em um gás)
2.
Qual das alternativas a seguir NÃO corresponde à uma propriedade dos coloides?
A – Efeito Tyndall
B – Movimento browniano
C – Natureza heterogênea
D – Instabilidade
A opção correta é a alternativa D – Instabilidade, uma vez que os coloides são muito estáveis.